基本信息
1、办理部门:广东省药品监督管理局
2、办理方式:网上办理
3、办理地点:广州市黄花岗街道东风东路753号之二一楼受理大厅
4、咨询电话:020-37886014 CIO咨询:400-003-0818
受理条件
符合以下条件的医疗机构可以提出申请:申请人取得拟变更的医疗机构制剂批准文号。
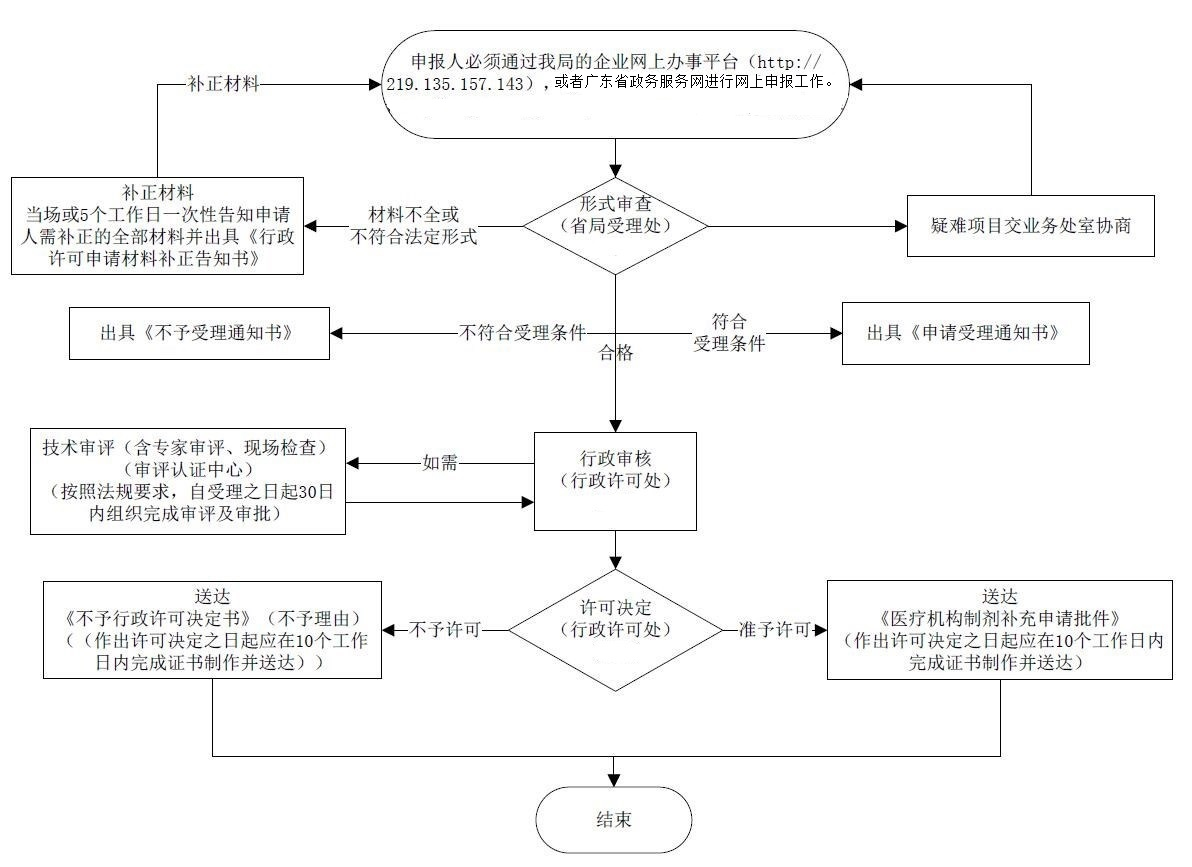
办理流程
流程文字说明
法定办结时限:20个工作日;承诺办结时限:1个工作日
1、受理(时限:5个工作日)
办理结果:1.能当场受理或通过当场补正达到受理条件的,直接进入受理步骤,当场出具受理通知书;2.根据一次性告知通知书内容进行补正后达到受理条件的,出具决定受理通知书;3.收件之日起5个工作日内未收到一次性告知通知书的,从收件之日起即为受理。
2、决定(时限:1个工作日)
办理结果:1.申请符合规定的,准予行政许可。 2.申请不符合规定的,不准予行政许可。
3、制证(时限:10个工作日)
办理结果:准予行政许可决定书 不准予行政许可决定书。
送达方式:网上发证、邮寄送达。
申请材料
1、医疗机构制剂注册补充申请申请表。
2、制剂批准证明文件及其附件的复印件。
3、《医疗机构执业许可证》复印件。
4、提供管理机构同意更名的文件复印件,更名前与更名后的《医疗机构执业许可证》、《医疗机构制剂许可证》的复印件。
结果样本
常见问题
问题1:我们想要进行质量标准提高,请问需要提前准备什么材料呢?
答:具体需要报送的材料见以下指南:http://www.gdzwfw.gov.cn/portal/guide/11440000MB2D034421244017200500309。
问题2:请问进行补充申请的申报需要多长时间呢?
答:自受理之日起,7个工作日内作出行政许可决定;自行政许可决定之日起10日内制证办结,并告知申请人。以上时限包括技术审查时间,不包括申请人补正资料、制证所需的时间。
问题3:我们配制单位地址发生了变更,但是配制单位名称没有发生改变需要进行补充申请吗?
答:需要。根据《广东省食品药品监督管理局医疗机构制剂注册管理办法(试行)实施细则》第二十七条第九款需要提出制剂补充申请的事项包括变更制剂配制场地。
问题4:我们想要变更质量标准直接接触药品的包装材料或容器需要准备什么材料呢?
答:具体需要报送的材料见以下指南:http://www.gdzwfw.gov.cn/portal/guide/11440000MB2D034421244017200500304。
问题5:办理补充申请许可业务需要收费吗?
答:不收费。根据《行政许可法》第五十八条行政机关实施行政许可和对行政许可事项进行监督检查,不得收取任何费用。但是,法律、行政法规另有规定的,依照其规定。行政机关提供行政许可申请书格式文本,不得收费。行政机关实施行政许可所需经费应当列入本行政机关的预算,由本级财政予以保障,按照批准的预算予以核拨。
问题6:请问我从哪里可以查到我的办理进度呢?
答:查询网址:http://219.135.157.143/gdyj/internet/spcx/SpcxYwsqList.faces。
问题7:我们对说明书内容进行了修改,请问需要办理补充申请吗?
答:需要。根据《广东省食品药品监督管理局医疗机构制剂注册管理办法(试行)实施细则》第二十七条第十款规定需要提出制剂补充申请的事项包括变更包装、标签、说明书。
问题8:如何查询我们即将选择的直接接触药品的包装材料是否符合标准?
答:请到国家药品监督管理局药品审评中心网站进行查询。
问题9:医疗机构制剂补充申请事项的相关问题?
答:咨询人可到省局公众网站公众参与网上咨询平台查阅常见问题。
本办事指南摘自药监局官网,如有变动,以官方发布为准。