基本信息
1、办理部门:江西省药品监督管理局
2、办理方式:网上办理
3、办理地点:江西省南昌市红谷滩区北龙蟠街993号方楼省政务服务中心三楼
4、咨询电话: 0791-86739757、0791-86739753 CIO咨询:400-003-0818
受理条件
符合食品药品监管总局关于加强中药生产中提取和提取物监督管理的通知(食药监药化监〔2014〕135号 )规定的条件和要求,申请材料齐全、符合法定形式,或者申请人按要求提交全部补充申请材料,即可办理。
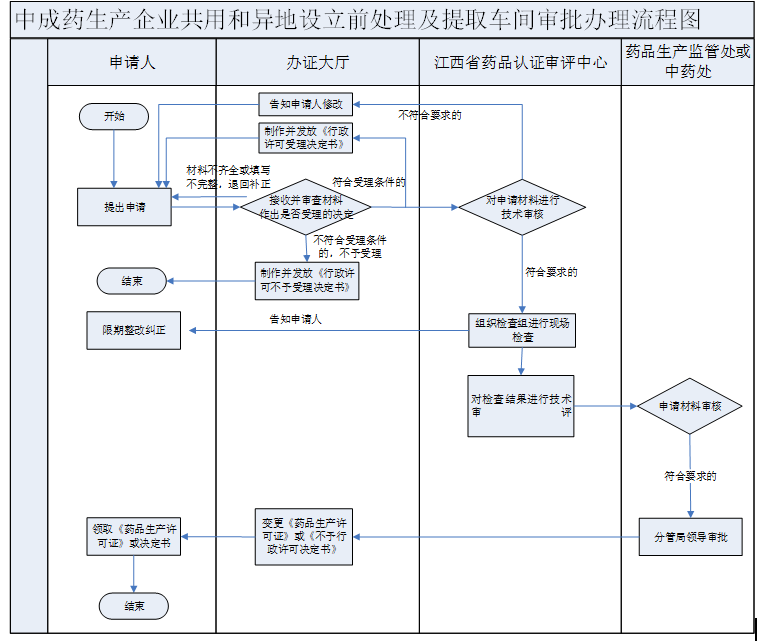
办理流程
流程文字说明
1、受理(时限:1个工作日)
办理结果:受理。
2、审查(时限:5个工作日)
办理结果:审查。
3、办结(时限:1个工作日)
办理结果:制证。
申请材料
2、双方《药品生产许可证》正副本复印件、营业执照正副本复印件;
3、双方《药品生产质量管理规范》认证证书复印件或药品GMP符合性检查结果告知书;
4、提供申请方与接受共用前处理和提取车间的药品生产企业同属于集团内部具有控股关系的药品生产企业说明;
5、跨省(区、市)设立共用车间的,需提供车间所在地省(区、市)药品监督管理局审查意见。跨省(区、市)设立异地车间的,需提供车间所在地省(区、市)药品监督管理局审查意见;
6、所涉品种的注册批件复印件、质量标准;中药提取物质量标准、工艺流程图、质量控制点;
7、申请方对共用车间的生产条件、技术水平和质量管理情况的考核报告。报告应至少包括以下内容:接受方的技术人员,厂房、设施、设备等生产条件和能力,以及质检机构、检测设备等质量保证体系能否满足提取物生产的需要;
8、共用车间合同:明确规定双方在中药提取物生产管理、质量控制等方面的质量责任及相关的技术事项,特别是要明确原辅料、包装材料的采购、检验和放行以及中药提取物检验、放行中双方各自的权利和义务,双方应共同建立对中药提取物生产活动的质量管理体系等内容,并符合国家有关药品管理的法律法规;
9、共用车间主要生产设备及检验仪器目录;
10、中药提取物所涉及的生产管理、质量管理文件目录;
11、试生产连续三批提取物检验合格报告(省或市药检机构);
12、申请人对其申请材料全部内容真实性保证的自我声明(见附件);
13、有关申请事项如果不是企业法人来办理,则要出具由法人签字并加盖企业公章的《授权委托书》;
14、企业的组织机构图(注明各部门的职责及相互关系、部门负责人)和异地设立车间组织机构图;异地设立车间依法经过资格认定的药学及相关专业技术人员、工程技术人员、技术工人登记表,并标明所在部门及岗位;高级、中级、初级技术人员的比例情况表;
15、异地设立车间的周边环境图、总平面布置图、仓储平面布置图、质量检验场所平面布置图、生产工艺布局平面图,空气净化系统的送风、回风、排风平面布置图,工艺设备平面布置图;
16、异地设立车间空气净化系统、制水系统、主要设备验证概况;生产、检验仪器、仪表、衡器校验情况;
17、异地设立车间主要生产设备及检验仪器目;
18、异地设立车间生产管理、质量管理文件目录;
19、有关委托检验协议复印件、洁净区的空气净化监测报告;
20、对照药品GMP相应条款,进行自查自评,形成自评报告;
21、企业确认接收《药品生产许可证》和《药品GMP证书》的邮寄地址、联系人、联系方式,盖企业公章并注明日期。
结果样本

常见问题
问题1:什么情况下申请不成功?
答:申请书未加盖公章;申请许可类别中类别名称、品种明细等出现错误;企业注册地址、社会信用代码填写与企业营业执照标注不一致。
本办事指南摘自药监局官网,如有变动,以官方发布为准。