基本信息
1. 办理部门:广东省药品监督管理局
2. 办理方式:网上办理
3. 办理地点:广州市黄花岗街道东风东路753号之二一楼受理大厅任一窗口
4. 药监咨询:020-37886014 CIO咨询:400-003-0818
受理条件
符合以下全部条件的医疗机构可以提出申请:
1.医疗机构制剂批准文号的持有单位;
2.已取得制剂批准文号的医疗机构如不再具备配制制剂的资格或者条件的,其化学药制剂批准文号自行废止,不参与制剂再注册;其中药制剂可参与制剂再注册。
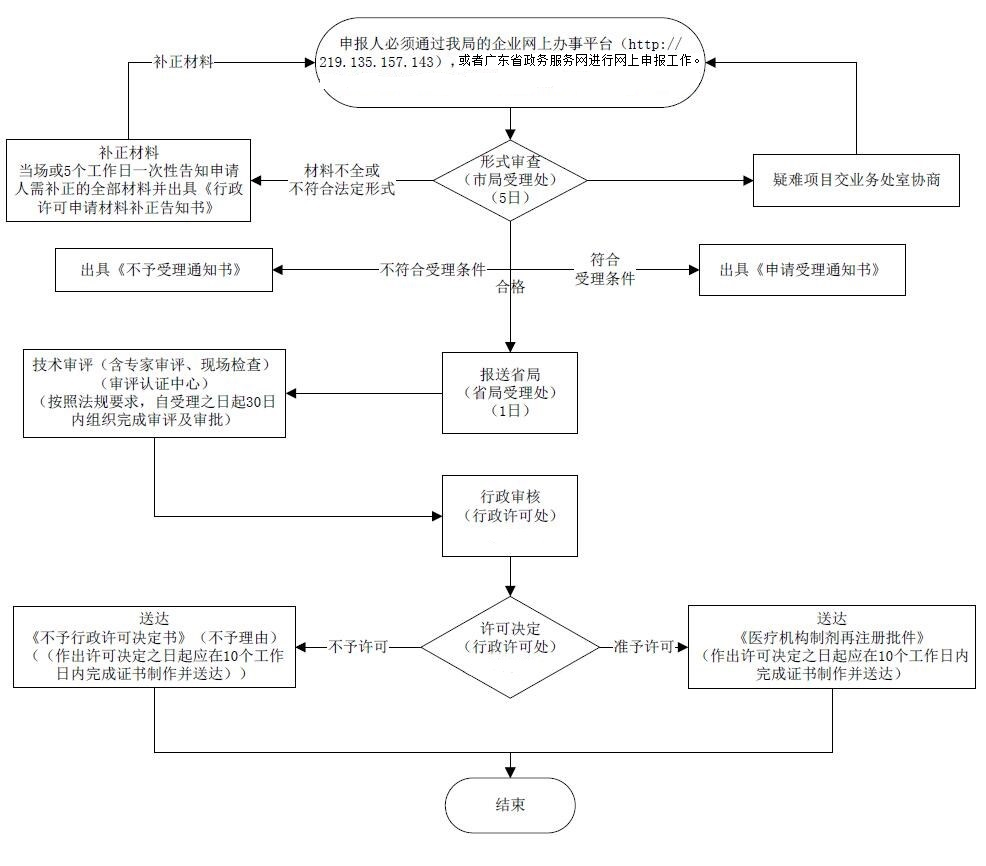
办理流程
流程文字说明
法定办结时限:30个工作日;承诺办结时限:8个工作日。
1.收件(时限:5个工作日)
办理结果:1.能当场受理或通过当场补正达到受理条件的,直接进入受理步骤,当场出具受理通知书;2.根据一次性告知通知书内容进行补正后达到受理条件的,出具决定受理通知书;3.收件之日起5个工作日内未收到一次性告知通知书的,从收件之日起即为受理。
2.审查(时限:4个工作日)
办理结果:提出初步意见,转入决定步骤。
3.决定(时限:4个工作日)
办理结果:1.申请符合规定的,准予行政许可。 2.申请不符合规定的,不准予行政许可。
4.制证(时限:10个工作日)
办理结果:准予行政许可决定书 不准予行政许可决定书。
申请材料
结果样本

常见问题
问题1:医疗机构制剂再注册事项的相关问题
答:咨询人可到省局公众网站公众参与网上咨询平台查阅常见问题。
问题2:需要提前多长时间进行再注册申请?
答:申请人应在批准文号有效期届满前3个月向所在地市食品药品监督管理局提出再注册申请。
问题3:再注册需要提交什么材料?
答:具体需要报送的材料见以下指南:http://www.gdzwfw.gov.cn/portal/guide/11440000MB2D0344212440172005002。
问题4:我们的制剂是委托配制的,除了常规的材料外,我们还需要提供什么材料呢?
答:委托配制的医疗机构中药制剂在提出再注册申请时还应提供以下资料:1)委托配制延期申请;2)前次委托配制期间,配制及制剂质量情况的总结;3)前次《医疗机构中药制剂委托配制批件》及其变更内容的证明文件。
问题5:我们收到了不予再注册批件,但是原来的批件还未过期,请问我们还能继续生产该制剂吗?
答:根据《医疗机构制剂注册管理办法(试行》 第三十四条的规定 已被注销批准文号的医疗机构制剂,不得配制和使用;已经配制的,由当地(食品)药品监督管理部门监督销毁或者处理。
问题6:请问不予再注册的原因有哪些呢?
答:根据《医疗机构制剂注册管理办法(试行》 第三十三条的规定 有下列情形之一的,省、自治区、直辖市(食品)药品监督管理部门不予批准再注册,并注销制剂批准文号:1)市场上已有供应的品种;2)按照本办法应予撤销批准文号的:3)其他不符合规定的。
问题7:请问再注册申请提交后多久能收到批件呢?
答:自受理之日起,8工作日内作出行政许可决定;自行政许可决定之日起10工作日内制证办结,并告知申请人。以上时限不包括申请人补正资料、技术审查所需的时间。
问题8:请问我从哪里可以查到我的办理进度呢?
答:查询网址:http://219.135.157.143/gdyj/internet/spcx/SpcxYwsqList.faces。
本办事指南摘自药监局官网,如有变动,以官方发布为准。