基本信息
1、办理部门:重庆市药品监督管理局
2、办理方式:窗口办理 网上办理 快递申请
3、办理地点:重庆市渝北区宝圣湖街道食品城大道27号重庆市药品监督管理局行政审批服务中心05-09号窗口
4、咨询电话:023-60353664 CIO咨询:400-003-0818
受理条件
1、医疗机构制剂的申请人,应当是持有《医疗机构执业许可证》并取得《医疗机构制剂许可证》的医疗机构。未取得《医疗机构制剂许可证》或者《医疗机构制剂许可证》无相应制剂剂型的“医院”类别的医疗机构可以申请医疗机构中药制剂,但是必须同时提出委托配制制剂的申请。接受委托配制的单位应当是取得《医疗机构制剂许可证》的医疗机构或者取得《药品生产许可证》的药品生产企业。委托配制的制剂剂型应当与受托方持有的《医疗机构制剂许可证》或者《药品生产许可证》所载明的范围一致。
2、医疗机构制剂注册分为制剂临床研究申请和制剂配制申请。新申请制剂一般应当先申请制剂临床研究,获批准并完成临床研究后,再申请制剂配制。
3、医疗机构配制的制剂,应当是本单位临床需要而市场上没有供应的品种。有下列情形之一的,不得作为医疗机构制剂申报:1.市场上已有供应的品种;2.含有未经国家药品监督管理部门批准的活性成分的品种;3.除变态反应原外的生物制品;4.中药注射剂;5.中药、化学药组成的复方制剂;6.麻醉药品、精神药品、医疗用毒性药品、放射性药品;7.其他不符合国家有关规定的制剂。
4、办理医疗机构制剂注册申请事务的人员应当是相应的专业技术人员,并且应当熟悉相关管理法律、法规和医疗机构制剂注册的技术要求。
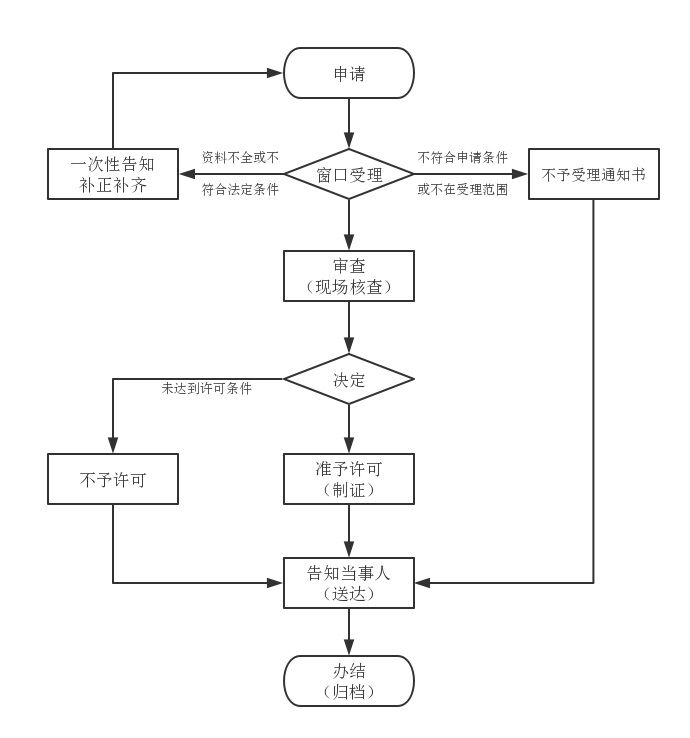
办理流程
流程文字说明
法定办理时限:20个工作日;承诺办理时限:10个工作日
1、受理(时限:0个工作日)
2、审查(时限:5个工作日)
3、决定(时限:5个工作日)
4、颁证(时限:0个工作日)
申请材料
1、配制工艺的研究资料及文献资料;
2、制剂的质量标准草案及起草说明;
3、直接接触制剂的包装材料和容器的选择依据及质量标准;
4、临床研究方案;
5、主要药效学试验资料及文献资料;
6、制剂名称及命名依据;
7、证明性文件;
8、处方组成、来源、理论依据以及使用背景情况;
9、样品的自检报告书;
10、质量研究的试验资料及文献资料;
11、立题目的以及该品种的市场供应情况;
12、急性毒性试验资料及文献资料;
13、长期毒性试验资料及文献资料;
14、原、辅料的来源及质量标准;
15、申报资料真实性承诺书;
16、医疗机构制剂注册申请表;
17、临床研究总结;
18、制剂的稳定性试验资料;
19、标签及说明书设计样稿。
结果样本

常见问题
问题1:未达到“医院”级别的中医门诊部(中医诊所)是否可以申请医疗机构制剂注册?
答:根据《重庆市医疗机构制剂注册补充规定》(渝食药监[2009]98号)的规定:未达到“医院”类别的中医诊所(含门诊部,下同)可以申请注册中药制剂,但必须符合以下条件: (1)必须是经卫生行政管理部门批准的中医医疗机构,有《医疗机构执业许可证》; (2)医疗机构已设立5年以上; (3)只能申请注册中药制剂; (4)不得申请注册注射剂等高风险剂型; (5)申请注册的中药制剂功能主治在《医疗机构执业许可证》所载明的诊疗范围内; (6)中药制剂必须委托已取得《医疗机构制剂许可证》的医疗机构或已取得《药品生产质量管理规范》认证证书的药品生产企业配制; (7)制剂品种不得调剂到本诊所以外使用。 2.什么情况下可以免于提交临床研究资料? 答:中药制剂:根据中医药理论组方,利用传统工艺配制(即制剂配制过程没有使原组方中治疗疾病的物质基础发生变化的),且该处方在本医疗机构具有5年以上(含5年)使用历史的中药制剂,可免报资料项14-18,即14.主要药效学试验资料及文献资料;15.急性毒性试验资料及文献资料;16.长期毒性试验资料及文献资料;17.临床研究方案;18.临床研究总结。 但是,如果有下列情况之一者需报送资料项目15、16: (1)处方组成含有法定标准中标识有毒性及现代毒理学证明有毒性的药材; (2)处方组成含有十八反、十九畏配伍禁忌; (3)处方中的药味用量超过药品标准规定的。 化学制剂:申请配制的化学制剂属已有同品种获得制剂批准文号的,可以免报资料项目14-18。
本办事指南摘自药监局官网,如有变动,以官方发布为准。

























