基本信息
1、办理部门:云南省药品监督管理局
2、办理方式:窗口办理、网上办理
3、办理地点:云南省昆明市高新区科发路616号云南省药品监督管理局一楼行政受理1号窗口。市内可乘85路、267路公交车到科发路口科高路站;116路、83路公车到科发路口(海源北路)站下车即到
4、咨询电话:0871-68571817/68571936/68571961 CIO咨询:400-003-0818
受理条件
1、医疗机构持有卫生行政主管部门的PET-CT或PET设备配置与使用许可证明文件《放射诊疗许可证》。
2、医疗机构制备正电子类放射性药品应当持有第III类以上(含第III类)《放射性药品使用许可证》。
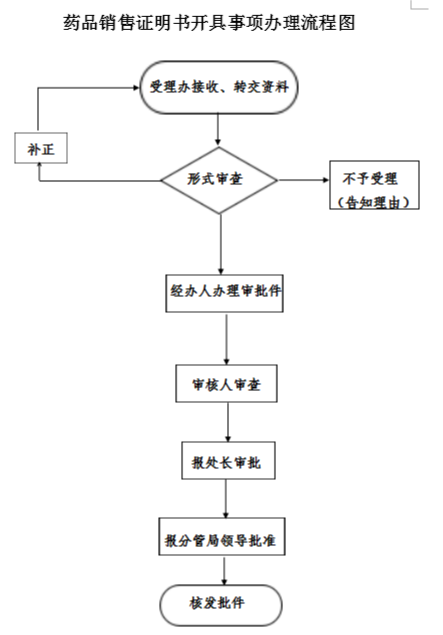
办理流程
流程文字说明
法定办理时限:20个工作日;承诺办理时限:8个工作日
1、申请
2、受理(时限:5个工作日)
3、审查(时限:6个工作日)
4、决定(时限:2个工作日)
5、送达
申请材料
1、医疗机构制备正电子类放射性药品申请表;
2、医疗机构《放射性同位素工作许可证》;
3、《医疗机构执业许可证》正副本;
4、医疗机构《放射性药品使用许可证》(第Ⅲ类或第Ⅳ类);
5、药品名称(通用名、化学名、英文名、汉语拼音药品名称(通用名、化学名、英文名、汉语拼音,自定义名称应说明命名依据));
6、药品化学结构、分子量、分子式;
7、立题依据(本品在国内外研制和应用情况的文献资料);
8、本品制备工艺研究资料及文献资料(包括放射性核素生产工艺,照射条件,核反应式),辐照后靶材料的化学处理工艺,可能产生的放射性核杂质,精制(纯化)方法,靶材料和所用化学试剂的规格标准及分析测试数据,本品合成路线,反应条件,精制或纯化方法;
9、质量标准(尚未有国家药品标准,制备该品种的医疗机构应起草质量标准并附起草说明,并经中国药品生物制品检定所复核);
10、三批成品的自检报告及常温下稳定性(三个半衰期)研究资料;
11、中国药品生物制品检定所或国家食品药品监督管理局授权的药品检验所对连续制备的三批样品的检验证书;
12、实验动物的靶器官及全身显像或模拟临床功能测定试验的研究方法,试验条件的资料,试验观察各时相的显像或功能测定结果;
13、医学伦理委员会的批件;
14、人体主要受照器官的医学内照辐射吸收剂量估算或国外相同品种的文献资料;
15、药品的说明书、包装、标签样稿;
16、《法人授权委托书》及被委托人身份证明;
17、申请材料真实性承诺书;
18、《放射诊疗许可证》。
结果样本

常见问题
无
本办事指南摘自药监局官网,如有变动,以官方发布为准。























