基本信息
1. 办理部门:浙江省药品监督管理局
2. 办理方式:网上申请,现场窗口申请,邮寄申请
3. 办理地点:浙江省杭州市莫干山路文北巷27号一楼受理大厅3号窗口
4. 药监咨询:0571-88903246 CIO咨询:400-003-0818
受理条件
具有生产含第二类精神药品的药品复方制剂或其他产品的资质。
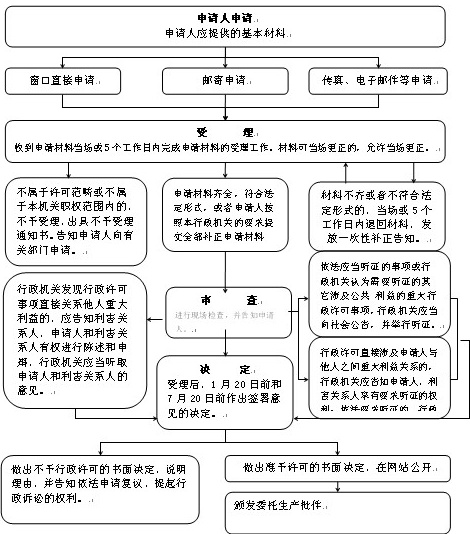
办理流程
流程文字说明
1、申请
申请人向登记(发照)机关窗口提交申请材料,或在浙江政务服务网进行网上申报,并选择结果送达方式。
2、受理(时限:5个工作日)
办理结果:(1)材料齐全符合法定形式的出具《受理通知书》;(2)材料不齐全或不符合法定形式的出具《补正告知书》;(3)不属于许可范畴或者不属于本机关受理范围的出具《不予受理通知书》。
3、现场检查/审查/核准和决定
办理时限:(1)每年11月底前上报下年度需用计划,次年1月20日前签署备案意见;
(2)每年5月底前申报年度补充计划,7月20日前签署备案意见。
办理结果:(1)申请人的申请材料符合法定条件,标准、审核通过的,出具核准、审批文件;(2)申请人的申请材料不符合法定条件、标准,审核不通过的,出具不予核准、审批文件。
4、送达(时限:10个工作日)
办理结果:根据申请人选择的送达方式送达结果文书。
申请材料
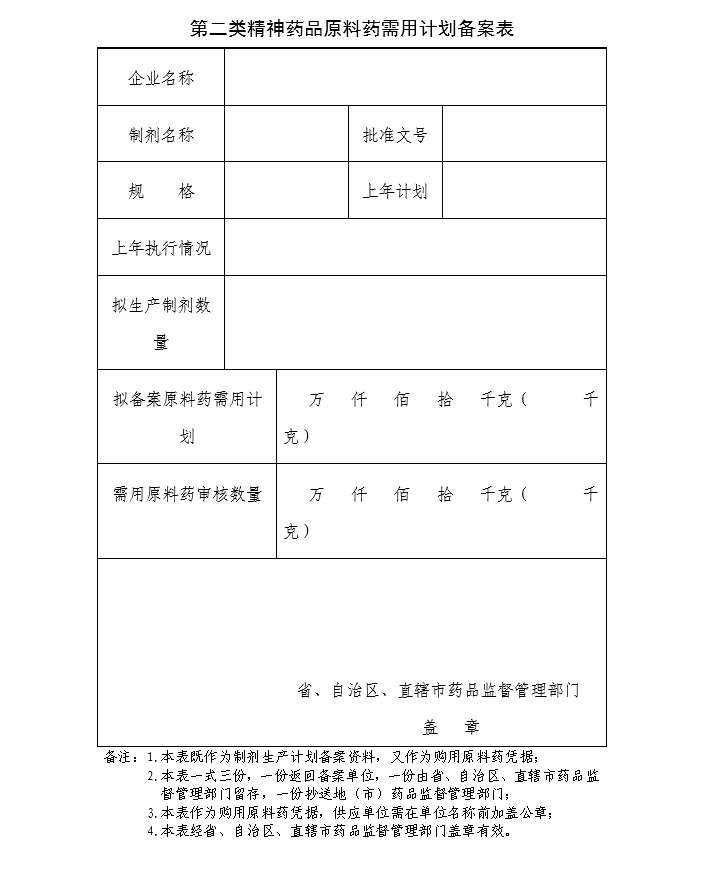
1、《第二类精神药品原料药需用计划备案表》(包含委托他人代办的法人签字的委托书及被委托人身份证复印件,以及申请材料真实性的保证声明,有法定代表人签字、企业公章、日期);>>第二类精神药品原料药需用计划备案表
2、《药品生产许可证》;
3、所生产药品批准证明文件;
4、相应剂型GMP符合性检查结果;
5、《营业执照》;
6、企业麻醉药品和精神药品管理的组织结构图;
7、企业总平面布置图、仓储平面布置图;
8、麻醉药品和精神药品生产工艺布局平面图、工艺设备平面布置图;
9、麻醉药品和精神药品安全管理制度文件目录。
结果样本
常见问题
问题1:申请药品生产企业使用第二类精神药品原料备案有什么要求?
答:受理条件具有生产含第二类精神药品的药品复方制剂或其他产品的资质。
本办事指南摘自药监局官网,如有变动,以官方发布为准。