 E邀专家
E邀专家
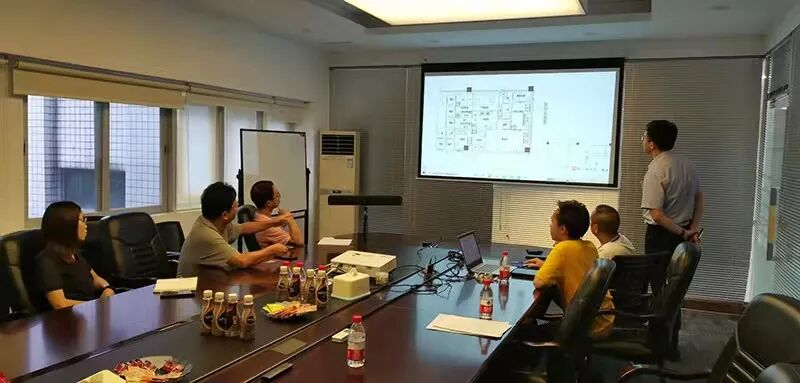
2026年3月30日,暨南大学附属第一医院传来振奋人心的消息——由广东暨德康民生物科技有限责任公司(以下简称暨德康民)自主研发的异体“γδ-T细胞注射液”I期临床试验正式启动。这是中国首个获批临床的γδ-T细胞创新免疫药物,也是全球首个针对实体瘤(晚期肝癌)的异体γδ-T细胞药物临床试验。
从2024年4月获得NMPA临床试验默示许可,到2026年3月I期临床正式启动,暨德康民用扎实的进展证明:中国创新药企完全有能力走通从实验室到临床的合规之路。

(照片来源于暨德康民公众号)
作为陪伴暨德康民走过合规体系建设关键阶段的合作伙伴,CIO合规保证组织与有荣焉,谨致以最热烈的祝贺!
l 我们CIO的作用:在关键爬坡期,帮助企业夯实GMP根基
时间回到2021年10月。当时的暨德康民,研发实力雄厚——首席科学家尹芝南教授从事γδT细胞研究二十余年,拥有核心专利技术。然而,从“优秀的实验室科学”走向“监管下的合格药品”,横亘着一道必须跨越的门槛:药品生产质量管理规范(GMP)体系。
彼时的挑战是系统性的:文件体系几乎从零开始,缺少一套符合NMPA申报要求的完整GMP文件框架;人员GMP意识亟待提升;硬件条件也需要按临床级标准进行验收。
2021年10月,CIO合规保证组织与暨德康民达成合作,为暨德康民提供覆盖GMP文件体系建立、人员培训、车间及检验室验收咨询的系统性合规服务。
我们主要开展了三方面的工作:一是结合暨德康民的产品特性和工艺特点,与暨德康民团队合作系统性搭建了符合IND申报要求的GMP文件体系;二是针对不同岗位开展分层培训,建立培训档案,确保人员资质与能力到位;三是对车间及检验室进行专业验收咨询,确保硬件条件符合IND申报标准。这套在关键爬坡期打下的GMP体系基础,为暨德康民后续的IND申报和临床试验启动提供了决定性支撑。

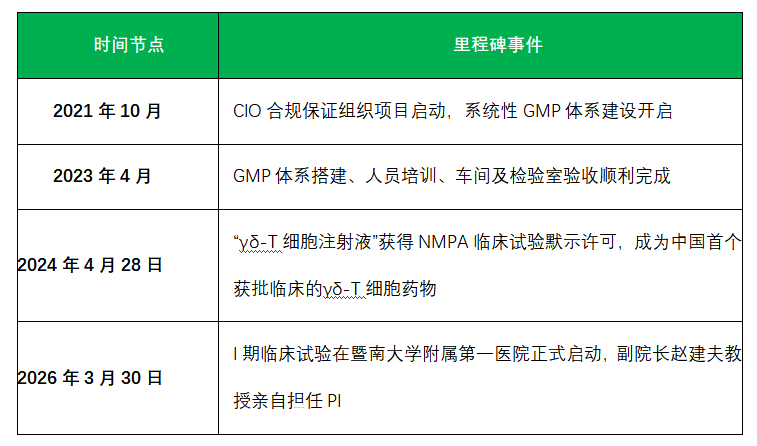
从CIO项目启动到I期临床启动,历时约四年半。这条清晰的时间线证明:合规不是创新的阻力,而是创新成果走向临床、造福患者的“高速公路”。
l CIO的定位:陪伴企业走过最关键的“合规爬坡期”
在细胞治疗这样的前沿领域,法规在演进,技术在迭代。合规服务的目标不是“通过一次检查”,而是帮助企业建立一套能够持续运行、自我优化的质量体系。这正是CIO合规保证组织一直践行的理念。我们不仅提供“标准答案”,更致力于与企业共同成长,使其在IND申报、临床试验、乃至未来商业化生产的每一个阶段,都能从容应对。
再次祝贺暨德康民!
期待“异体γδ-T细胞注射液”在临床试验中取得优异结果,早日为晚期肝癌患者带来新的治疗希望。
CIO合规保证组织将继续以“促进医药产业合规、助力企业高质量发展”为使命,陪伴更多中国创新药企,走通从实验室到临床的合规之路。
讯息链接:
《走进暨德康民,CIO合规保证组织为生物细胞治疗领域研发创新加力》(暨德康民公众号,2021年10月)
《重磅!全球领先的针对实体瘤的γδ-T细胞药物临床试验登陆广州,肝癌患者将迎来免疫治疗新选择》(暨德康民公众号,2026年4月1日)
 E邀专家
E邀专家
最新推荐
热门观点

药械企业法律风险预防与应对闭门研讨会

医疗器械注册/备案、变更

合规破局与价值重塑 医药营销转型实战训练营

医疗器械生产许可申请/变更

化妆品注册/备案、变更

药品(国产/进口)注册、变更

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

原辅包注册/登记

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

药品经营许可申请 / 变更

执业药师继教服务

药物警戒第三方委托服务

医药企业涉刑防范与应对

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

化妆品生产许可申请/变更

药械企业法律风险预防与应对闭门研讨会

医疗器械注册/备案、变更

合规破局与价值重塑 医药营销转型实战训练营

医疗器械生产许可申请/变更

化妆品注册/备案、变更

药品(国产/进口)注册、变更





