 E邀专家
E邀专家
2026年3月9日,广东省药品监督管理局颁发了一张引人注目的B类药品生产许可证(编号:粤20260008)。持证方为正清海琴(珠海横琴)科技有限公司,受托方为湖南正清制药集团股份有限公司,证书备注栏明确标注:“用于持有人转让”。
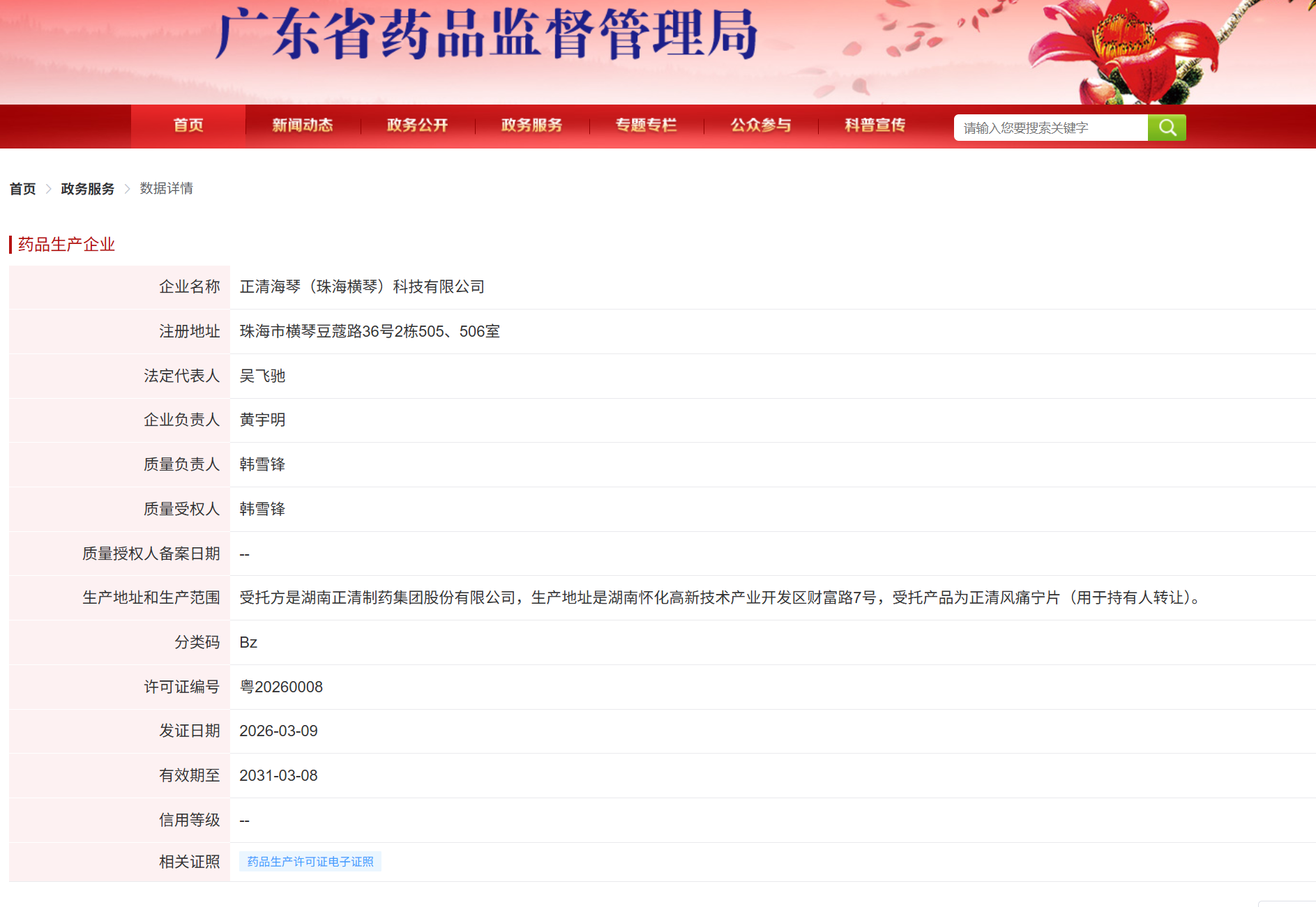
这是2026年广东省公开的首张以“持有人转让”为由获批的B证。在过去两年,业界普遍反映广东省对于跨省委托、单纯买卖批文的B证审批极为审慎。这张证书的落地,释放了怎样的监管信号?结合2023年132号公告与2026年初发布的134号公告,我们或许可以窥见MAH监管的新逻辑。
一、案例解读:正清海琴B证为何能“破冰”?
这张证书的特殊性,在于其精准契合了当前监管政策的多重考量。
Ø 集团内转让,契合政策导向
134号公告第三条明确规定:“在同一集团内执行统一质量管理体系的企业之间委托生产药品的,可简化持有人资质、质量管理能力等评估内容”。正清海琴与受托方湖南正清制药存在股权关联,属于典型的集团内部资源整合。监管层通过这一案例传递的信号是:集团内部的产业布局调整,在合规前提下,通道始终畅通。
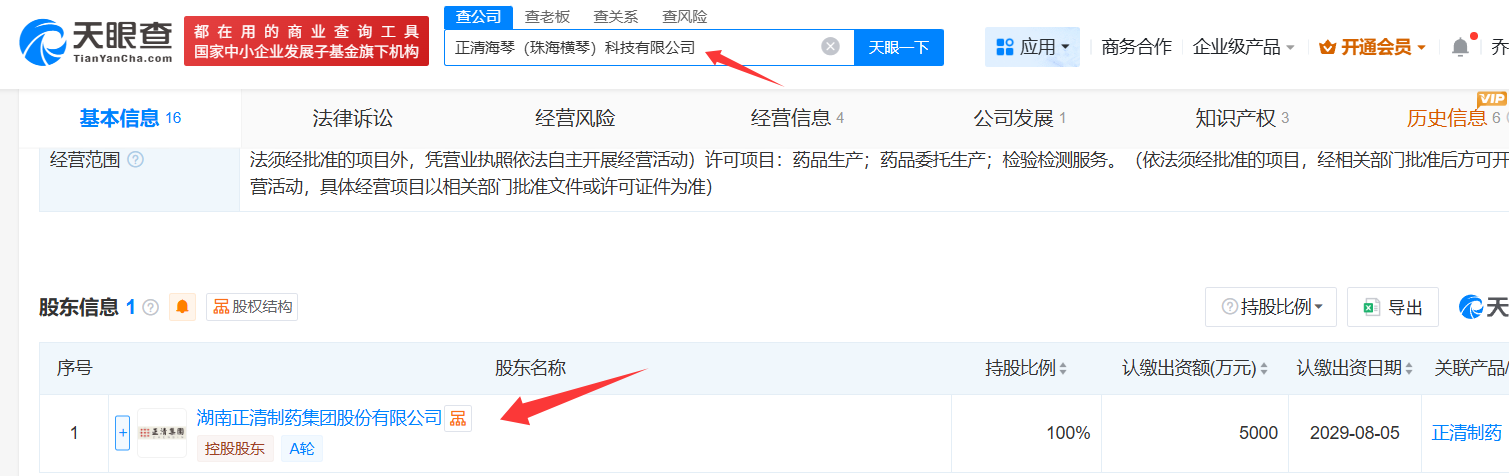
(图示:经天眼查查询“正清海琴(珠海横琴)科技有限公司”是“湖南正清制药集团股份有限公司”的全资子公司)
Ø 品种成熟,风险可控
“正清风痛宁片”是上市多年的中药老品种,不属于132号公告重点监管的中药注射剂、多组分生化药等高风险品类。临床数据扎实,工艺稳定,不存在研发阶段的未知变量。对于此类成熟品种的持有人变更,技术审评的逻辑与高风险品种自然不同。这印证了监管的严格程度与品种风险正相关的基本逻辑。
Ø 跨省委托,检验协同机制
132号公告明确提出跨省委托的监管分工:持有人所在地省局负责持有人监管,受托方所在地省局负责受托方监管。正清海琴注册在广东、生产在湖南的模式,正是对这一跨省协同机制的实际检验。证书的顺利颁发,证明广东与湖南两省药监部门在实践中能够建立起顺畅的监管协作。
Ø 产业布局真实,回应“空壳”焦虑
新持有人落地横琴粤澳深度合作区,符合大湾区中医药高地建设规划,具备实质性运营基础。这回应了监管部门对“空壳B证”的一贯关注——无论是132号公告还是134号公告,其核心逻辑都是压实责任,确保持有人具备履行质量安全职责的能力。
二、政策脉络:从132号到134号,监管逻辑的重构
理解这张B证的深层意义,需要看清近年来委托生产监管的演进脉络。
l 132号公告:给持有人戴上“紧箍咒”
2023年10月发布的132号公告,从“严格委托生产的许可管理”和“强化委托生产的质量管理”两方面入手,对持有人提出了前所未有的细化要求。委托生产无菌药品的,关键人员必须具备无菌药品管理经验;对于高风险品种,设置更严格的前置研究条件。132号公告标志着监管重点从“持有人自身能力”向“持有人对受托方的管理能力”延伸——不仅要自己懂,还要能管好帮你生产的人。
l 134号公告:让受托方站到聚光灯下
2026年1月6日发布的134号公告,是这场监管升级的“最后一块拼图”。它首次将监管视角对称地投向受托生产企业,核心目的是督促双方“共同履行保障药品质量安全的主体责任”。受托方不再是单纯的“代工”执行者,而是与持有人法律地位平等、责任共担的质量安全共同体。
134号公告要求受托方在接受委托前必须对持有人进行全面评估,建立涵盖偏差、变更、药物警戒等信息的质量沟通程序,在发现风险时有权暂停生产并报告监管部门。这彻底改变了以往仅由持有人评估受托方的单向模式,建立了双向选择、相互制衡的新机制。
三、监管新逻辑:从“单边管理”到“双边共治”
正清海琴B证的落地,折射出监管框架的三个深刻变化。
逻辑一:质量管理能力是双向门槛
134号文让受托方从被动的“乙方”成为质量责任的“共治方”。受托方在接受委托前,必须对持有人的质量管理能力进行评估。这意味着:质量管理体系不健全的持有人,在实践中可能面临“找不到代工厂”的困境。市场选择机制与监管要求在此处形成合力。
逻辑二:过程耦合比准入更重要
134号文不仅关注“能不能委托”,更关注“委托后怎么管”。它要求委托双方必须建立质量沟通程序,涵盖偏差处理、变更控制、稳定性考察、投诉与不良反应、召回等所有关键环节。这种“过程耦合”的要求,考验的是双方质量管理体系的协同能力,而不仅仅是持有一张许可证。
逻辑三:跨省协同走向常态化
134号文进一步明确了跨省委托的监管协调机制:两地省局建立信息通报和联合检查机制。正清海琴这张B证,正是这一机制落地的实证。它告诉行业:跨省委托不是监管盲区,而是需要更精细设计的合规路径。
四、行业启示:B证企业的合规新课题
正清海琴B证的落地,对正在筹划或已经持有B证的企业,提出了一些值得深思的课题。
课题一:质量管理能力是“入场券”而非“加分项”
134号文要求受托方在接受委托前评估持有人的质量管理能力。这意味着,质量管理能力直接决定企业能否找到合作伙伴。持有人需要建立覆盖全生命周期的质量管理体系,而不仅仅是满足发证审查的“纸面合规”。关键人员的资质、质量协议的深度、偏差处理的机制,都将成为受托方评估的重点。
课题二:跨省委托需“双重合规”思维
对于跨省委托的企业,需要同时满足持有人所在地和受托方所在地的监管要求,同时应对两地药监部门的检查。这要求企业对两地监管规则都有充分理解,并建立与之相适应的内部管理机制。单纯依赖某一方的合规思维,可能难以应对跨省监管的复杂性。
课题三:集团内部整合迎来政策窗口
134号文对集团内委托的简化评估条款,为大型药企优化产业布局提供了便利。正清海琴的案例证明,这一通道在实践中是可操作的。对于拥有多地布局的企业而言,这是一个值得关注的战略方向——将研发、销售、生产职能在集团内重新配置,既符合监管导向,也有助于提升运营效率。
五、结语
从132号文到134号文,国家药监局用两年时间,构建了一个更加清晰的委托生产监管框架。其核心逻辑是:通过明确且对称的责任划分,将MAH制度下的质量责任,有效地传导至委托生产的每一个环节。持有人和受托方,从此成为共同承担质量安全责任的利益共同体。
正清海琴B证的落地,证明了在这一监管框架中,合规的持有人转让通道是畅通的。它向行业传递的信息是:规则越清晰,合规者的路径越明确。
对于那些正在筹划B证申请或持有人变更的企业而言,与其焦虑政策变化,不如静下心来审视自己的质量管理体系是否经得起132号文和134号文的检验。毕竟,在MAH制度下,许可证是起点,真正支撑企业持续发展的,是那张证书背后扎实的质量管理能力。
(CIO合规保证组织专注于医药领域合规研究,致力于提供专业的医药准入咨询和GMP合规服务。本文仅代表专家个人观点,供行业参考。)
 E邀专家
E邀专家





















