基本信息
1、办理部门:湖南省药品监督管理局
2、办理方式:网上办理
3、办理地点:长沙市天心区银杏路6号政务服务大厅一楼B19-B26窗口
4、咨询电话:0731-82213687 CIO咨询:400-003-0818
受理条件
1.符合《医疗器械监督管理条例》中第一百零三条及《体外诊断试剂注册与备案管理办法》第三条的定义;
2.属于《体外诊断试剂分类规则》及《体外诊断试剂分类子目录》中第二类体外诊断试剂的范围;
3.注册申请人及申报资料符合《体外诊断试剂注册与备案管理办法》第二、三章的规定;
4.符合《医疗器械说明书和标签管理规定》的规定;
5.符合《医疗器械生产质量管理规范》及其相关附录的要求。
6.办理医疗器械注册事项的人员应当具有相应的专业知识,熟悉医疗器械注册管理的法律、法规、规章和注册管理相关规定。
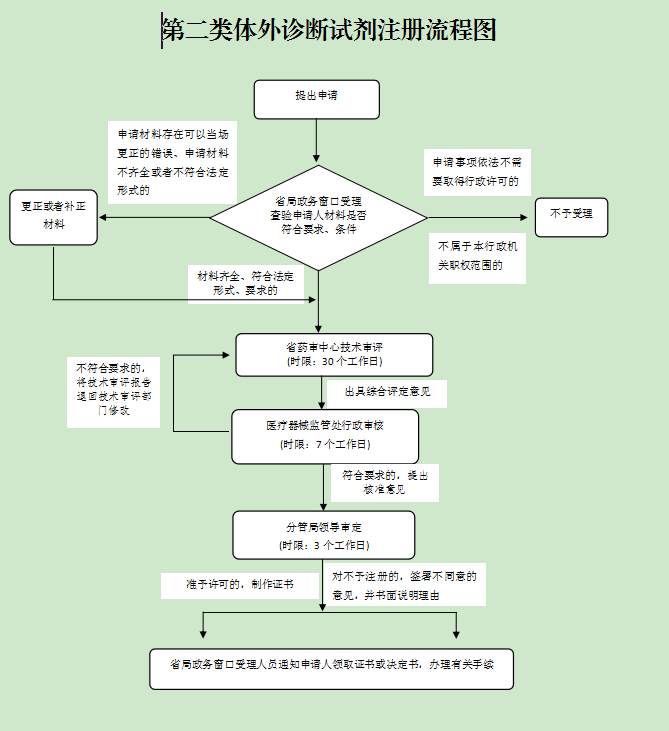
办理流程
流程文字说明
法定办结时限:140个工作日;承诺办结时限:70个工作日。
1、受理:0个工作日
2、缴费:0个工作日
3、技术审评:40个工作日
4、行政审核:7个工作日
5、行政审定:3个工作日
>>委托办理咨询 体外诊断试剂注册证核发
申请材料
1、《湖南省第二类医疗器械注册申请表》;>>申请表
2、监管信息;
3、综述资料;
4、非临床资料;
5、临床评价资料;
6、产品说明书和标签样稿;
7、质量管理体系文件。
结果样本

常见问题
问题1:申请第二类医疗器械产品注册向什么部门提交注册申请资料?
答:根据《医疗器械监督管理条例》(2000年1月4日国务院令第276号,2014年3月7日予以修改)第十一条:申请第二类医疗器械产品注册,注册申请人应当向所在地省、自治区、直辖市人民政府食品药品监督管理部门提交注册申请资料。……
本办事指南摘自药监局官网,如有变动,以官方发布为准。