基本信息
1、办理部门:安徽省药品监督管理局
2、办理方式:网上办理、窗口办理
3、办理地点:安徽省合肥市包河区马鞍山路509号安徽省政务服务中心1号办事大厅企业开办综合窗口
4、咨询电话:0551-62999882、0551-62999795 CIO咨询:400-003-0818
受理条件
一、申请人为安徽省内市场主体,且无被限制进入药品行业的情形。
二、符合《药品生产监督管理办法》第六条规定的条件:
(一)有依法经过资格认定的药学技术人员、工程技术人员及相应的技术工人,法定代表人、企业负责人、生产管理负责人(以下称生产负责人)、质量管理负责人(以下称质量负责人)、质量受权人及其相他关人员符合《药品管理法》《疫苗管理法》规定的条件;
(二)有与药品生产相适应的厂房、设施、设备和卫生环境;
(三)有能对所生产药品进行质量管理和质量检验的机构、人员;
(四)有能对所生产药品进行质量管理和质量检验的必要的仪器设备;
(五)有保证药品质量的规章制度,并符合药品生产质量管理规范要求。
从事疫苗生产活动的,还应当具备下列条件:
(一)具备适度规模和足够的产能储备;
(二)具有保证生物安全的制度和设施、设备;
(三)符合疾病预防、控制需要。
三、申请人应当符合《药品管理法》《疫苗管理法》等法律法规和《国家药监局关于加强药品上市许可持有人委托生产监督管理工作的公告》(2023年第132号)等有关要求。
四、申请材料(具体见申请材料目录)齐全、符合形式审查要求,或者申请人按照要求提交全部补正材料的,予以受理。
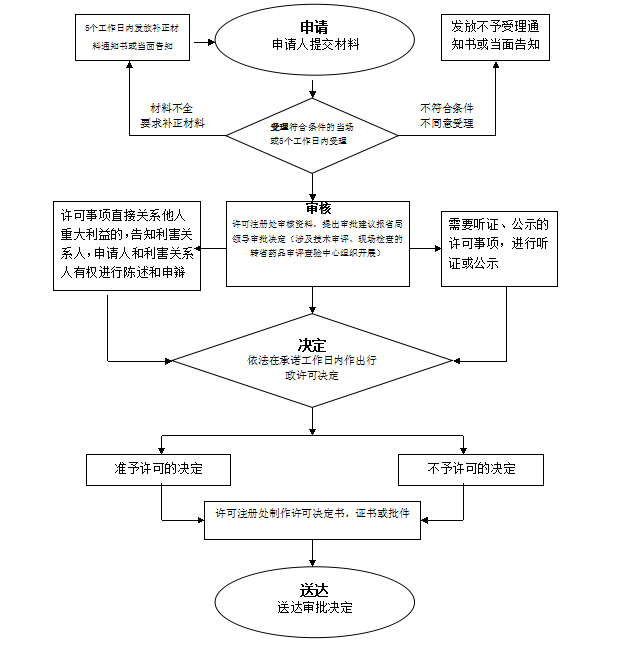
办理流程
流程文字说明
法定办理时限:30个工作日;承诺办理时限:20个工作日
1、受理(时限:1个工作日)
2、审查(时限:17个工作日)
3、决定(时限:1个工作日)
4、办结(时限:1个工作日)
申请材料
药品上市许可持有人自行生产的情形:
1、药品生产许可证申请表;>>药品生产许可证申请表
2、基本情况;
3、企业的情况说明;
4、组织机构图;
5、关键人员情况等证明性材料;
6、技术人员登记表;
7、高级、中级、初级技术人员的比例情况表;
8、周边环境图平面布置图;
9、生产工艺布局平面图、空气净化系统送风回风排风平面布置图、工艺设备平面布置图;
10、拟生产的情况;
11、拟生产剂型品种的工艺流程图;
12、确认验证校验情况;
13、主要生产设备检验仪器目录;
14、生产管理质量管理主要文件目录;
15、药品出厂上市放行规程;
16、申请材料全部内容真实性承诺书;
17、授权委托书;
18、疫苗的储存运输管理情况。
药品上市许可持有人委托他人生产的情形:
1、药品生产许可证申请表;>>药品生产许可证申请表
2、基本情况;
3、组织机构图;
4、关键人员情况等证明性材料;
5、技术人员登记表;
6、高级、中级、初级技术人员的比例情况表;
7、拟委托生产的情况;
8、拟委托生产剂型品种的工艺流程图;
9、生产管理质量管理主要文件目录;
10、药品上市放行规程;
11、委托协议质量协议;
12、持有人确认受托方具有受托生产条件技术水平质量管理能力的评估报告;
13、受托方药品生产许可证正副本;
14、受托方药品生产企业的情况说明;
15、受托方周边环境图平面布置图;
16、受托方生产工艺布局平面图、空气净化系统送风回风排风平面布置图、工艺设备平面布置图;
17、受托方确认验证校验情况;
18、受托方主要生产设备检验仪器目录;
19、受托方药品出厂放行规程;
20、受托方所在地省级药品监管部门出具的通过药品GMP符合性检查告知书;
21、受托方所在地省级药品监管部门出具的同意受托生产的意见;
22、申请材料全部内容真实性承诺书;
23、授权委托书。
药品生产企业接受委托生产的情形:
1、药品生产许可证申请表;>>药品生产许可证申请表
2、基本情况;
3、企业的情况说明;
4、组织机构图;
5、关键人员情况等证明性材料;
6、技术人员登记表;
7、高级、中级、初级技术人员的比例情况表;
8、周边环境图平面布置图;
9、生产工艺布局平面图、空气净化系统送风回风排风平面布置图、工艺设备平面布置图;
10、拟接受委托生产的情况;
11、拟接受委托生产剂型品种的工艺流程图;
12、确认验证校验情况;
13、主要生产设备检验仪器目录;
14、生产管理质量管理主要文件目录;
15、药品出厂放行规程;
16、委托协议质量协议;
17、申请材料全部内容真实性承诺书;
18、授权委托书。
原料药生产企业的情形:
1、药品生产许可证申请表;>>药品生产许可证申请表
2、基本情况;
3、企业的情况说明;
4、组织机构图;
5、关键人员情况等证明性材料;
6、技术人员登记表;
7、高级、中级、初级技术人员的比例情况表;
8、周边环境图平面布置图;
9、生产工艺布局平面图、空气净化系统送风回风排风平面布置图、工艺设备平面布置图;
10、拟生产的品种质量标准及依据;
11、拟生产品种的工艺流程图;
12、确认验证校验情况;
13、主要生产设备检验仪器目录;
14、生产管理质量管理主要文件目录;
15、药品出厂放行规程;
16、申请材料全部内容真实性承诺书;
17、授权委托书。
结果样本


常见问题
问题1:药品生产许可证上的法定代表人能不能不和营业执照上的法定代表人为同一人?
答:药品生产许可证上的法定代表人依据营业执照确定。
问题2:药品生产许可证有效期有多长?
答:药品生产许可证有效期为5年。
问题3:生产药用辅料需要办理药品生产许可证吗?
答:无需办理。
问题4:企业在申请药品生产许可过程中,如果提交虚假资料从而获得药品生产许可证,会不会受到处罚?
答:依据《药品管理法》第一百二十三条,提供虚假的证明、数据、资料、样品或者采取其他手段骗取药品生产许可的,撤销相关许可,十年内不受理其相应申请,并处五十万元以上五百万元以下的罚款;情节严重的,对法定代表人、主要负责人、直接负责的主管人员和其他责任人员,处二万元以上二十万元以下的罚款,十年内禁止从事药品生产经营活动,并可以由公安机关处五日以上十五日以下的拘留。
问题5:能否不按照《国家药监局关于加强药品上市许可持有人委托生产监督管理工作的公告》的要求进行B证核发的办理?
答:不能。
本办事指南摘自药监局官网,如有变动,以官方发布为准。

























