基本信息
1、办理部门:河北省药品监督管理局
2、办理方式:网上办理
3、办理地点:河北省石家庄市新华区石清路9号省政务服务大厅1号楼二层综合受理区综合受理窗口
4、咨询电话:0311-66635315 CIO咨询:400-003-0818
受理条件
《体外诊断试剂注册与备案管理办法》(国家市场监督管理总局令第48号)
第七十八条 注册人应当主动开展体外诊断试剂上市后研究,对体外诊断试剂的安全性、有效性和质量可控性进行进一步确认,加强对已上市体外诊断试剂的持续管理。 已注册的第二类、第三类体外诊断试剂产品,其设计、原材料、生产工艺、适用范围、使用方法等发生实质性变化,有可能影响该体外诊断试剂安全、有效的,注册人应当向原注册部门申请办理变更注册手续;发生其他变化的,应当在变化之日起30日内向原注册部门备案。 注册证载明的产品名称、包装规格、主要组成成分、预期用途、产品技术要求、产品说明书、进口体外诊断试剂的生产地址等,属于前款规定的需要办理变更注册的事项。注册人名称和住所、代理人名称和住所等,属于前款规定的需要备案的事项。境内体外诊断试剂生产地址变更的,注册人应当在办理相应的生产许可变更后办理备案。 发生其他变化的,注册人应当按照质量管理体系要求做好相关工作,并按照规定向药品监督管理部门报告。
第七十九条 已注册的第二类、第三类体外诊断试剂,产品的核心技术原理等发生实质性改变,或者发生其他重大改变、对产品安全有效性产生重大影响,实质上构成新的产品的,不属于本章规定的变更申请事项,应当按照注册申请的规定办理。
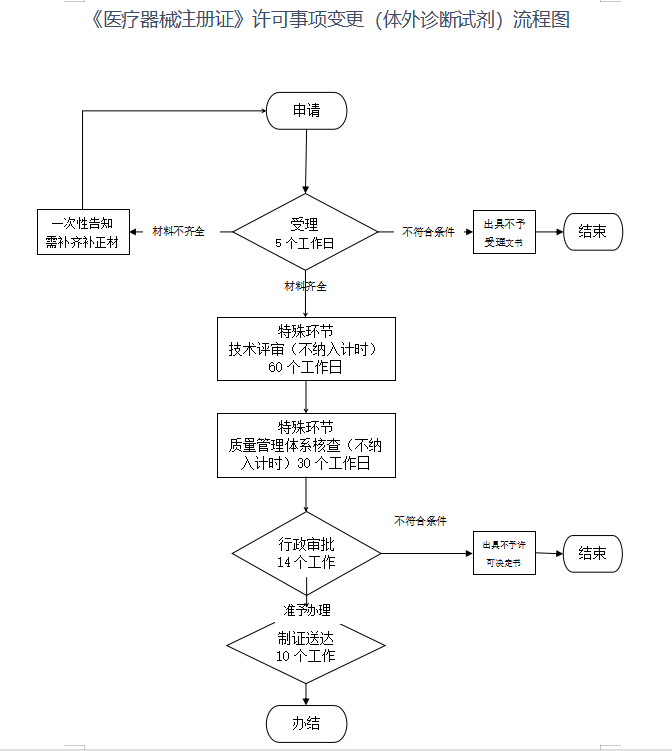
办理流程
流程文字说明
法定办理时限:35个工作日;承诺办理时限:19个工作日
1、受理(时限:5个工作日)
2、技术审评(时限:60个工作日,不纳入计时)
3、质量管理体系核查(时限:30个工作日,不纳入计时)
4、行政审批(时限:14个工作日)
5、制证、送达(时限:10个工作日,不纳入计时)
申请材料
1、监管信息;
2、综述资料;
3、非临床资料;
4、临床评价资料;
5、产品说明书;
6、质量管理体系文件。
结果样本

常见问题
问题1:办理该项业务需要哪些材料?
答:具体需要哪些材料在服务指南中有详细的说明。
本办事指南摘自药监局官网,如有变动,以官方发布为准。























