 E邀专家
E邀专家
本文将本人在CMAC(China Medical Advance Committee,中国医学发展促进委员会)2023年年度大会上分享的话题-非肿瘤药物临床开发样本量考量及美欧中实践整理成文字稿,供读者们参考。内容主要包括三方面:非肿瘤药物研发概况、慢病药物临床开发重要指导原则ICHE1、以及FDA、EMA及中国实践。
非肿瘤药物研发概况
美国在2013-2022年,FDA CDER平均每年批准43种新药;新药定义为新分子实体或新适应症或新人群。First-in-class占比呈上升趋势。First-in-class定义为与现有治疗的作用机制不相同。2022年,CDER批准了37种新药;First-in-class占比与2021年相当,占54%, 其中70%为非肿瘤适应症。FIC包括心肌病、糖尿病和银屑病等等。2022年美国65%的创新药获得至少1种加快审评程序,包括fast track, BTD, 优先审评以及加速审评。其中非肿瘤创新药占41%。

中国2022年获批1类创新药按ATC分布来看,抗肿瘤和免疫机能调节药占25%, 而非肿瘤心血管系统药物占16.7%,消化及代谢16.7%,神经系统16.7%, 呼吸、生殖泌尿以及系统抗感染药分别都占16.7%。整体非肿瘤药物占75%。2022年CDE将49个品种注册申请纳入优先审评程序。非肿瘤药物占67%。2022年CDE将39个品种注册申请纳入突破性治疗药物程序,涉及非小细胞肺癌、脊髓性肌萎缩症和胃癌等适应症。非肿瘤药物占38%。
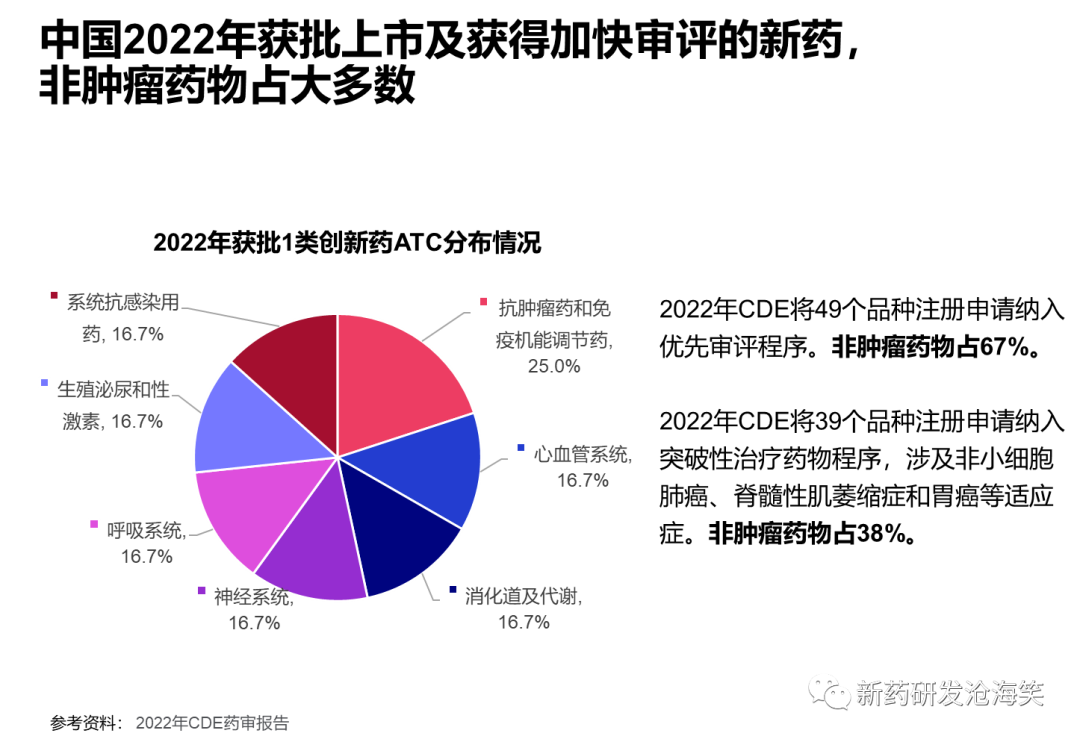
由此可见,无论是美国还是中国,近年来批准的新药中非肿瘤药物占大多数,而获加快程序的非肿瘤药物的占比也比较高。
ICHE1指导原则
慢病药物临床开发的一个重要指导原则是ICHE1,2022年11月后递交的NDA申请适用,这个时间已过,E1在中国已经实施。E1是一个经典的ICH指导原则,它的篇幅不是很长,一共三页的字,但是涵盖的信息量却非常大,博大精深。
E1是“人群暴露程度:评价无生命威胁条件下长期治疗药物的临床安全性”。题目包括3个关键词:1)人群暴露程度,意思是样本量和研究时长,这是企业非常关心的,因为涉及到临床开发的费用及时长。2)无生命威胁条件下长期治疗,这是E1的适用范围,无生命威胁,像高血压、糖尿病、高脂血症,高尿酸血症等属于这个范畴,而肿瘤以及其他危及生命的疾病不属于该范畴。长期治疗的定义是要超过6个月的慢性或者间断性使用。3)第三个关键信息临床安全性,E1是一个安全性指导原则,这是监管非常关注的。
E1内容主要包括一般考虑原则、总体协定内容。
一般考虑原则:
1)在临床药物研发期间的安全性评价要求能定性和定量描述与意求的药物长期使用相一致的一段合理时间内药物的安全性特征。定性就是也就是我们在临床试验中要看研发中的药物会出现什么样的不良事件或者不良反应,定量就是不良事件或者不良反应的频率怎么样?我们要通过试验把它们检验出来的。对于这个时间的跨度,它的要求是一个合理的时间内,这段合理的时间应该是要能够较好的预测药物在上市后患者长期使用时的安全性特点。对于长期慢性用药的品种,什么样的时间跨度能够合理的预测长期用药的情况?ICHE1在后面的总体的内容里面有具体的规定,主要是6个月与12个月。
2)为了能够达到定性和定量描述药物的安全性特征,需要一个合理的数据库。药物暴露的持续时间及其与不良事件发生的时间和严重性的关系是考虑要点。举例说,GLP-1的GIAE主要发生在开始用药的前3个月,之后逐渐减少或消失,对于这样的不良事件,监管总的来说不是那么担忧。但如果治疗一年或更长时间,如果引起抑郁或自杀事件的话,那么监管就会关注。
3)区分数据是来源于较短期的暴露还是较长期的暴露。也就是这个药物的不良事件是在给药后几个月或者说比较短的时间内出现的,还是在要一年或者是比较长的给药时间出现的,这对临床实际用药是很有帮助的。比如减肥药物纳曲酮,长期使用会增加心血管事件的风险,不过,分析心血管事件与时间的关系后,短期使用是安全的,所以说明书上加了仅限使用3个月说明。
4)如果发生率在一段时间内是变化的,应该根据不良事件的强度及其对药物风险-获益评价的重要性来描述。举个例子来说,辉瑞未上市的pcsk9单抗,使用3个月后,ADA和中和抗体的发生率增加,注射部位反应也增加。治疗1年后,降脂疗效减弱。综合评估风险及获益后,辉瑞决定不上市。
5)还有一个原则,“临床期间的安全性评价并不要求描述罕见不良事件的特征(如<0.1%)”。一般不要求描述罕见的不良事件,比如说要观察不良事件小于千分之1的,因为如果你要去描述这个罕见事件的样本量,可能要求的样本量特别的大,代价很大。
6)对于一个具体的临床试验来说,我们要去描述药物安全性的特征,三个方面是我们主要考虑:一个临床试验的设计是怎样的,暴露时间要多长,以及不同暴露时间下样本量要求多少?E1对试验设计做了一个总体的原则性的表述,描述了不同的试验设计,对不良事件和药物的因果关系的判断力做了一个总体的描述。对于暴露时间的长度,还有不同时暴露时间的样本量要求,E1做了一个比较详细的规定。根据以往对药物不良事件(ADE)的发生及观察经验,测定ADE特定频率概率的统计学考虑以及实际的考虑。三个时间节点很重要:累计暴露总数;6个月;1年。
关于研究设计,良好的设计可保证药物与不良事件之间的因果关系具有好的判断力。最好的就是安慰剂对照,因为安慰剂对照能将治疗组的不良事件发生率与研究人群不良事件的背景发生率进行直接比较。监管是比较乐于看见安慰剂对照,因为它证据级别强,如果高于安慰剂,那么不良事件和药物的关系可能是监管高度关注的,因为可能是药物相关的。除了安慰剂对照,接下来就是阳性对照或者活性对照,也是比较常见的一个设计。它可以比较药物间的不良反应发生率,但是它的缺点是不能直接评价药物研究人群不良事件的背景发生率。不过在这种试验设计也是可以把不良反应进行比较,试验药物和对照药相比,安全性比阳性对照的风险高了还是低了?有没有出现一个特别的安全性风险?这对于监管的审评也是有帮助的,只不过是和安慰剂比较,因果关系的判断没有那么强。有一种既包括安慰剂,也包括阳性对照的研究设计,双盲双模拟,既可以与背景发生率进行比较,也可以和阳性对照比较,不过,操作起来比较困难,因为除了自身的安慰剂,还需有阳性对照的安慰剂。下一个就是不设同期的对照,这种情况就是我们常常说的单臂开放设计研究,这种情况我们是难以评价药物和不良事件的因果关系的。还有一个就是说我们长期暴露的研究,通常都是一些扩展研究,多数都是非同期对照的开放性研究。

总体协定内容
1)暴露总数,经研究药物治疗的个体总数(包括短期暴露)的期望值约为1500;目前日本的接受为500-1500病患:较少的病患数量存在的可能是由于上市后药物的研究要求。在中国,累计暴露总数期望1500。这个包括健康受试者,即使用药1次也算。
2)6个月暴露数,已获知的信息显示极大部分ADE在药物治疗的最初几个月首次出现,而且最为频繁;以临床预期使用的剂量水平治疗一定数量的病患共6个月,病患的数量应足以描述这段时期内不良事件的特征。ICHE1制定的时候,基于前期经验,统计学考虑以及实际的考虑,最终ICHE1确定对于暴露6个月的样本量是300~600。6个月暴露的安全性是监管非常关注的。
3)1年暴露数,由于一些不良事件随时间的延长其频率和强度也增加;一些严重不良事件可能仅在药物治疗6个月后发生。因此,一些病患的治疗时间应持续至12个月。需100名病患接受药物暴露至少1年的安全性评价数据库(前瞻性)。在1年的药物暴露期间如果没有观测到严重ADE,那么这一病人数量可以保证1年累计真实发生率不大于3%。
例外情况,也就是需要更大、更长或更小数据库的情况。当药物将导致迟发ADE或随时间的延长强度或频率增加的ADE时,以及当需要对一个预期低频率的特定ADE的发生率作定量描述时,需要更大和更长的数据库。当药物获益: (1)太小;(2)接受治疗的病患仅有一部分能够体验(预防性治疗);(3)大小仍未确定(替代终点),决定风险/获益关系时,当药物可能增加本身就存在着显著的死亡率或发病率情况时,需要更大的数据库。目标治疗人群数量较小时,接受较小的病患数量,根据具体适应症而定,需与监管机构沟通。
总协定内容-NDA,根据治疗6个月的病患数据提出新药许可申请通常是合理的;在美国和日本,经12个月治疗的病患数据一经获得必须立刻呈交,并且必须在获得新药许可之前呈交。在美国,那些被确定为优先药物(priority drugs)的药物,其首次递交的申请中必须包括经12个月治疗的病患数据。欧洲国家,12个月数据的递交可以在获得新药许可之后。中国:一般情况下,NDA时需递交12个月的数据。
整体而言,ICHE1是最低要求,临床试验实践需要高于这个标准。1年暴露:需100名病患接受药物暴露至少1年的安全性评价数据库(前瞻性);6个月暴露:预期临床使用的剂量水平暴露300~600例;整体暴露:1500例。存在例外的情况,需与监管沟通。慢病领域常规的NDA申请,需要递交1年的有效性及安全性数据。
美国、欧盟及中国E1实践分析
美国的E1实践分析。这个研究分析了2002年10月1日-2014年12月31日美国FDA CDER批准NMEs及NTBs。. 参考资料为FDA clinical review。上市前暴露人数的计算:接受至少1次研究用药的受试者,排除健康受试者、安慰剂及阳性对照药。患者在早期研究中如在后期也参加研究只计算1次。研究结果显示,美国新药临床开发非罕见病药安全性样本量中位数为1600例,>1500例,满足E1的要求。再来看根据ATC分类的情况,整体53%非罕见病药物临床开发样本量>1500例,其中神经系统和呼吸系统最高,80%以上满足1500例。其次是心血管和生殖泌尿性激素,70%以上,之后是消化代谢60%以上。再看一下暴露6个月和1年的情况,6个月暴露>300例的非罕见病占91%, 暴露1年样本量>100的占90%,也就是大部分都满足E1的标准。
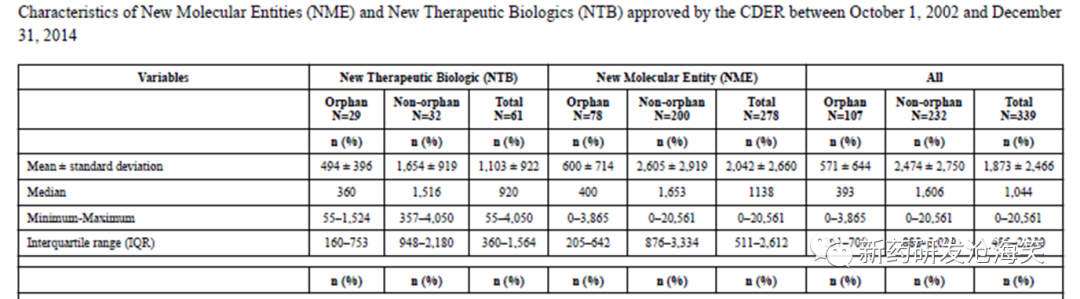
美国关键临床研究的设计情况。这个研究比较1995-1997,2005-2007及2015-2017美国FDA 批准NME及NTB关键临床研究特征。数据来源:Drugs@FDA database。研究发现,关键临床的设计以1.随机双盲安慰剂对照设计居多;2. 替代终点占大多数。另外,1. 关键临床研究非加速途径样本量及研究时长呈上升趋势,2. 获加速路径的研究样本量相对少。
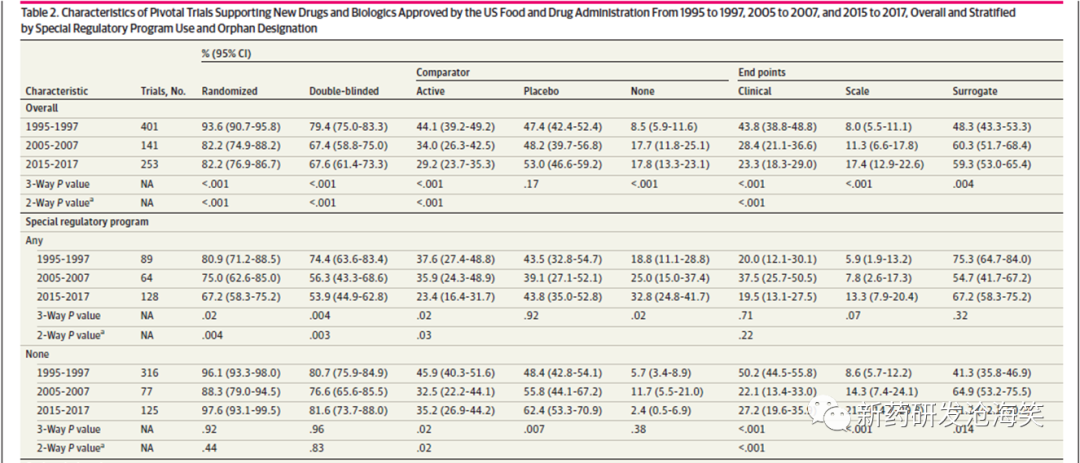
美国E1执行情况:1)非罕见病药物临床开发的样本量中位数为1606;2)满足ICHE1要求1500例的非罕见病药为53%,罕见病为7.5%;3)暴露6个月>300例及12个月>100例 比例≥90%;4)获加速路径的样本量相对少,但研究时长未变。
欧盟的E1实践分析。这个研究分析了EMA2000-2010年通过集中程序批准的新药数据。暴露以接受至少一次给药计算,包括健康受试者。慢病比如哮喘、HIV,间断治疗比如肿瘤。短期治疗比如抗菌、镇痛、诊断。欧盟慢病样本量为2338,间断治疗为800,短期治疗为1300,罕见病为400,整体平均是1300。慢病的样本量是最大的,高于美国以及E1的标准。EMA临床开发慢病非罕见病整体暴露量在1000-5000的比例居多。其中2000-5000占45%,1000-2000占27%。暴露6个月样本量300-1000占39%,样本量>1000占46%。而暴露1年样本量100-1000占53%,>1000占30%。也就是80%以上暴露6个月和1年的样本量满足E1的要求。
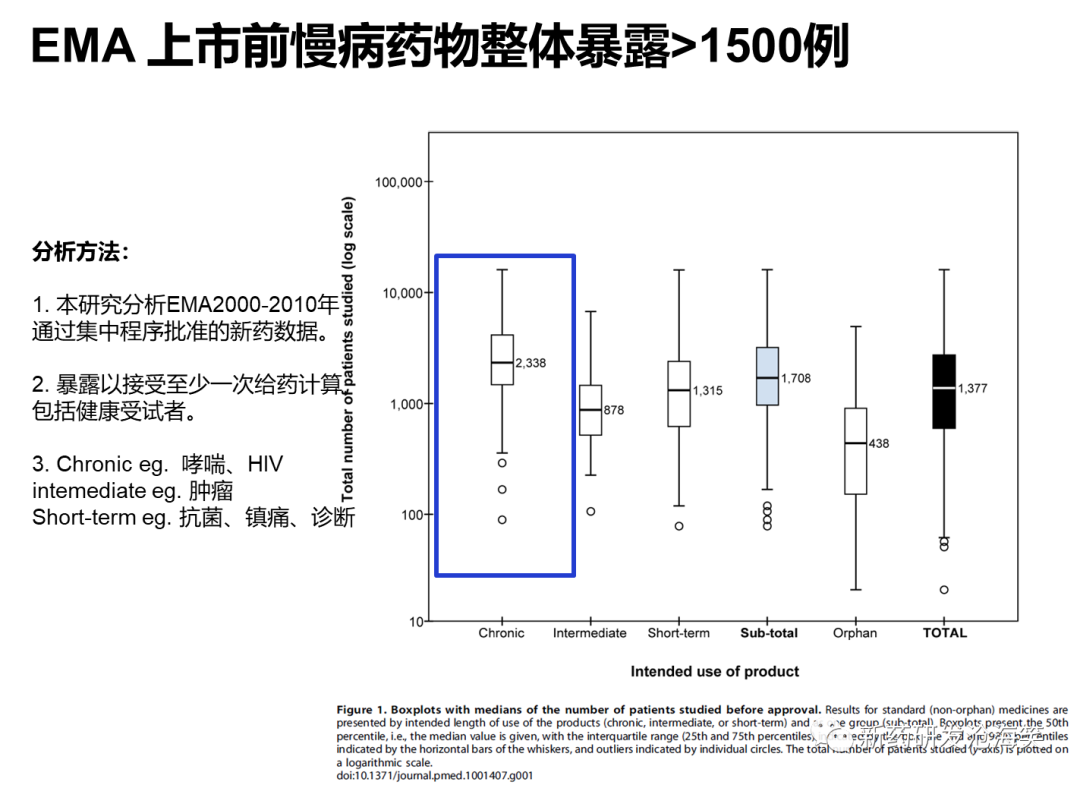
欧盟E1执行情况:1)EMA慢病临床开发样本量为2300;2)慢病非罕见病整体暴露量在1000-5000例的居多;3)暴露6个月患者数>300例,,暴露12个月患者数>100例的比例皆大于80%。FDA&EMA大部分慢病药物上市前安全性暴露超越或满足E1的要求。
中国的E1实践分析以及应对策略。中国E1尽管刚落地,但是有的企业已经率先执行了。比如恒格列净、海博迈步。泰它西普是例外情况。
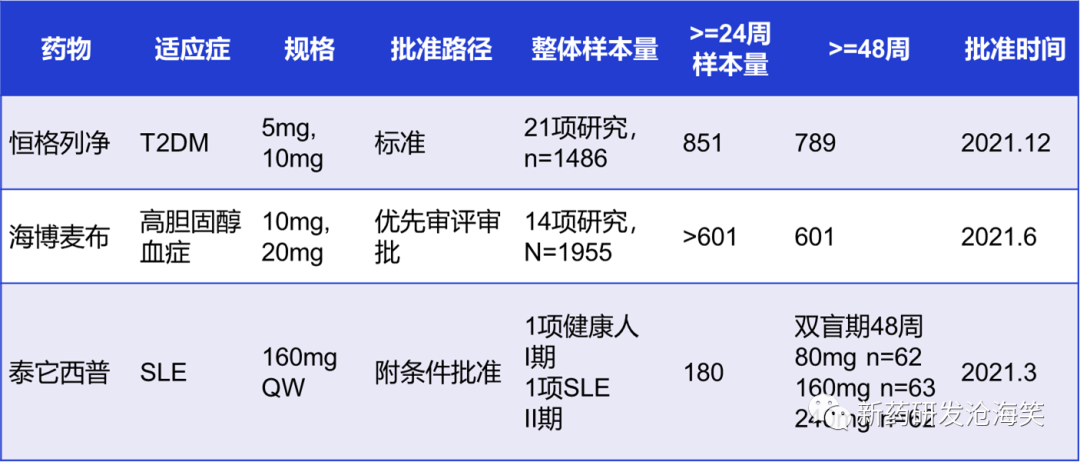
ICHE1对中国企业的挑战以及应对策略。挑战在于:1)临床开发样本量增大,2. 临床研究周期延长,3. 开发成本显著增加。应对策略:1. 基于临床价值,需挖掘创新点,建立竞争优势,获得附条件批准,BTD或优先审评审批;2. 根据疾病的特点,与监管沟通,争取政策支持,获得接受样本量较小、加速及缩短研究周期的处理;3. 早期开发可能需要考虑引入阳性对照,明确定位,及时止损;4.开发策略考虑全球;5. 真实世界研究与证据,可能会在未来的产品开发中起到越来越重要的作用。
*本文转载自微信公众号 - - 新药研发沧海笑
相关文件下载、服务及学习课程:
合规培训:AAV基因治疗产品CMC开发的合规实践
委托定制:药品生产许可证办理
联系专家,获取专家指导意见:e邀专家
*以上文章仅代表作者个人观点
 E邀专家
E邀专家



















