 E邀专家
E邀专家
在现代制药行业中,遵循GMP(药品生产质量管理规范)进行洁净厂房的设计是确保产品安全性和质量的关键。随着全球对药物质量和安全性的要求日益严格,洁净厂房的设计和建设成为药企满足监管要求、保障消费者健康的重要环节。本文将深入探讨如何设计一个既符合国家标准又能满足实际生产需要的理想空间,重点介绍GMP药厂设计的核心要素。
设计目的:创建无污染的生产环境
GMP药厂设计的核心目的是构建一个受控的生产环境,以防止产品受到外界污染物的影响,并避免交叉污染、混淆和差错的发生。通过实施严格的环境控制措施,确保所有生产活动都在最优化条件下进行,从而保证产品的安全性。洁净厂房不仅为员工提供了安全的工作场所,也为高质量药品的生产奠定了基础。
设计原则:法规遵从与流程适应性
GMP药厂的设计必须严格遵守2010版GMP及相关的《指导原则》,并要与具体的产品生产工艺和生产规模相匹配。合理的人员流动和物料运输路径规划对于减少污染风险至关重要。此外,适宜的照明、温度、湿度和通风条件也是保持产品质量稳定的重要因素。这些原则确保了生产的连续性和一致性,同时保护了操作人员的健康和安全。
工程项目设计采用的主要标准、规范
为了确保药厂的安全性和功能性,洁净厂房的设计需符合一系列国家标准和行业规定,例如:
•《建筑设计防火规范》(GB 50016-2014)
•《医药工业洁净厂房设计标准》(GB 50457-2019)
•《工业建筑供暖通风与空气调节设计规范》(GB 50019-2015)
这些标准和技术指南为洁净厂房的设计提供了坚实的技术支持,确保其能够有效地服务于药品生产的高标准需求。
洁净度等级与标准
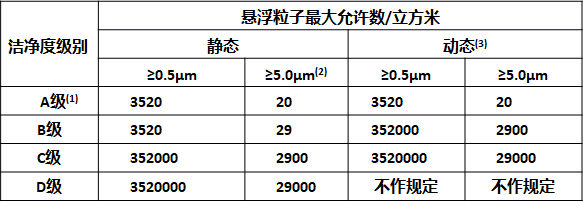
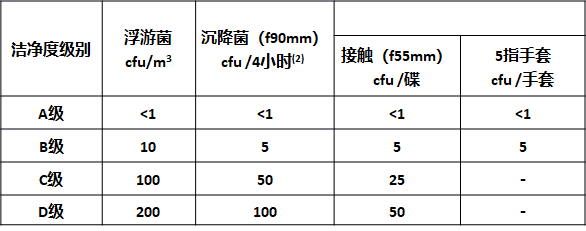
根据不同的工艺需求,洁净区被划分为多个级别,如百级(A级)到十万级(D级),每一级别都有其特定的微粒和微生物含量限制。这不仅符合GMP的要求,也确保了空气中的污染物处于最低水平。通过精准的洁净度管理,药厂可以维持稳定的生产环境,保障药品的质量和安全。
设计流程:从概念到施工
洁净厂房的设计过程通常包括三个阶段:概念设计、方案设计和施工图设计。每个阶段都紧密围绕总图布局和工艺平面展开,确保设计方案既科学又实用。良好的前期规划能够有效减少后期施工中的问题,提高项目的整体效率。
“五化”设计理念:打造现代化洁净药厂
为了实现高效、环保且人性化的生产环境,GMP药厂的设计还融入了“五化”的理念:
1.人性化:以员工的需求为中心,提供舒适的工作环境。
2.短平化:简化操作流程,提升工作效率。
3.节能化:采用节能环保材料和技术,降低能耗。
4.智能化:引入智能控制系统,增强管理效率。
5.自动化:应用自动化设备,提高生产精度和速度。
综上所述,设计符合GMP标准的洁净药厂不仅是制药企业合规运营的基础,更是提升产品质量、保护消费者健康的有力保障。通过精心设计和严格管理,我们可以构建出既符合国家标准又能满足实际生产需要的理想空间。选择专业的设计团队和可靠的合作伙伴,是成功建设GMP药厂的关键步骤之一。
相关文件下载、服务及学习课程:
合规文库:药品生产质量管理规范(2010年修订)
合规培训:新厂筹建项目管理与风险控制
委托定制:药厂筹建服务
联系专家,获取专家指导意见:e邀专家
*以上文章仅代表作者个人观点。
 E邀专家
E邀专家
最新推荐
热门观点

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

药械企业法律风险预防与应对闭门会

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

医药企业涉刑防范与应对

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训






