基本信息
1、办理部门:广东省药品监督管理局
2、办理方式:网上办理
3、办理地点:广州市黄花岗街道东风东路753号之二一楼受理大厅
4、咨询电话:020-37886014 CIO咨询:400-003-0818
受理条件
按《国家食品药品监管总局关于出口欧盟原料药证明文件有关事项的通知》要求。
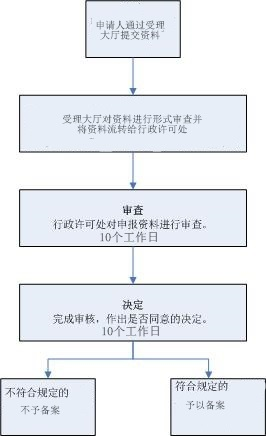
办理流程
流程文字说明
法定办结时限:20个工作日;承诺办结时限:20个工作日
1、申请
实行无纸化申报,可登录广东省政务服务网进行网上申报工作,填报申请事项材料,证明材料以扫描件上传。所有申报资料内容必须真实、合法,文字、图案清楚;电子扫描件需加盖申请人印章,为pdf扫描件,每个文件大小不能超过10M,按照系统要求上传至办事平台
2、资料接收
受理大厅收到申请材料后,作出资料接收或不予接收决定。申请材料不齐全或者不符合法定形式的,当场或者在5日内一次告知申请人需要补正的全部内容,逾期不告知的,自收到申请材料之日起即为受理。
3、受理(特别程序:实地核查,30个工作日)
实施机关对申请资料进行形式审查。申请被受理的,申请人可获得实施机关出具的受理凭证;申请不被受理的,申请人可获得实施机关出具的不予受理通知书,不予受理通知书的内容包括不予受理的理由。
4、获取结果
申请人可登录广东省药品监督管理局公众网首页审批查询栏进行办理进度查询,登录企业申报端获取电子证书。
送达方式:窗口领取、代理人送达、委托送达、公告送达、邮寄送达。
申请材料
1、出口欧盟原料药证明文件申请书。
2、该品种与国外采购企业的销售合同复印件。
3、该品种近3年获得其他国家或组织的药品GMP证书复印件。
4、我国药品监管部门发给的药品批准证明文件复印件。
5、《药品生产许可证》、企业营业执照(可通过系统自动获取)。
6、该品种的中国《药品GMP证书》复印件。
结果样本


常见问题
无
本办事指南摘自药监局官网,如有变动,以官方发布为准。

























