基本信息
1、办理部门:湖南省药品监督管理局
2、办理方式:窗口申请,网上办理
3、办理地点:湖南省长沙市天心区银杏路6号政务服务大厅一楼B19-B26窗口
4、咨询电话:0731-82213687 CIO咨询:400-003-0818
受理条件
(一)申请人必须持有《药品生产许可证》、《营业执照》;
(二)申请人必须持有该品种的药品注册证;
(三)符合《药品注册管理办法》(国家食品药品监督管理局局令第28号)的规定。
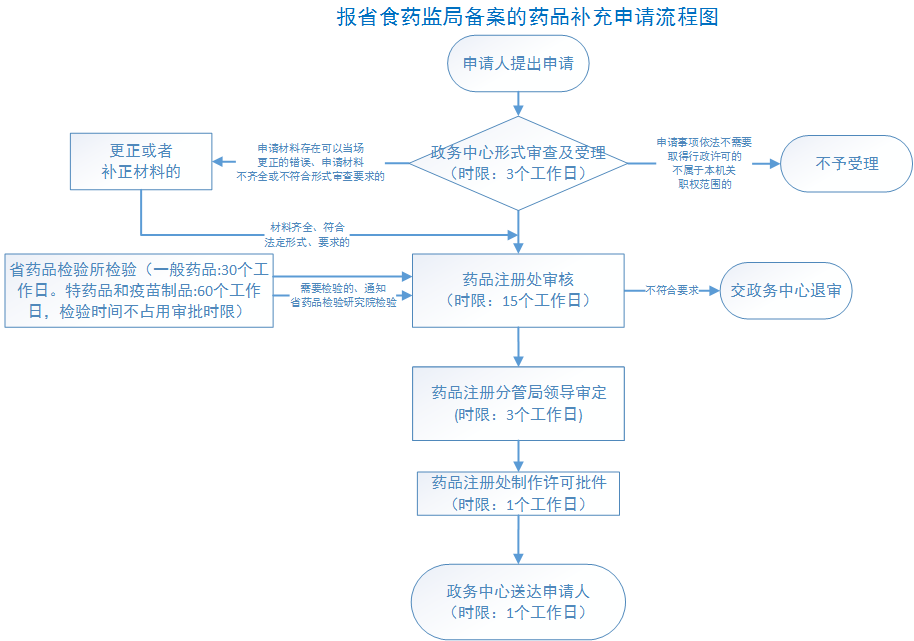
办理流程
流程文字说明
法定办结时限:35个工作日;承诺办结时限:23个工作日。
1、受理
2、资料审查:3个工作日
3、审核:15个工作日
4、审定:3个工作日
5、公告(办结):2个工作日
申请材料
1、修订的药品说明书和药品标签样稿;
2、药学研究资料;
3、临床试验资料;
4、药理毒理研究资料;
5、证明性文件;
6、药品补充申请表;
7、药品批件及所附质量标准,历次药品再注册批件及补充申请批件。
结果样本
常见问题
问题1:国产药品不改变药品内在质量的补充申请的受理部门是什么?
答:《中华人民共和国药品管理法实施条例》(2002年8月4日国务院令第360号,2016年2月6日予以修改)第三十二条:变更研制新药、生产药品和进口药品已获批准证明文件及其附件中载明事项的,应当向国务院药品监督管理部门提出补充申请;国务院药品监督管理部门经审核符合规定的,应当予以批准。其中,不改变药品内在质量的,应当向省、自治区、直辖市人民政府药品监督管理部门提出补充申请;省、自治区、直辖市人民政府药品监督管理部门经审核符合规定的,应当予以批准,并报国务院药品监督管理部门备案。不改变药品内在质量的补充申请事项由国务院药品监督管理部门制定。
本办事指南摘自药监局官网,如有变动,以官方发布为准。