基本信息
1、办理部门:国家药品监督管理局
2、办理方式:窗口办理,网上办理,快递申请
3、办理地点:北京市丰台区南四环西路188号12区29号楼
4、药监咨询:010-53815833 CIO咨询:400-003-0818
受理条件
申请事项属于本行政机关职权范围,申请材料齐全、符合法定形式,或者申请人按照本行政机关的要求提交全部补正申请材料的,受理行政许可申请。
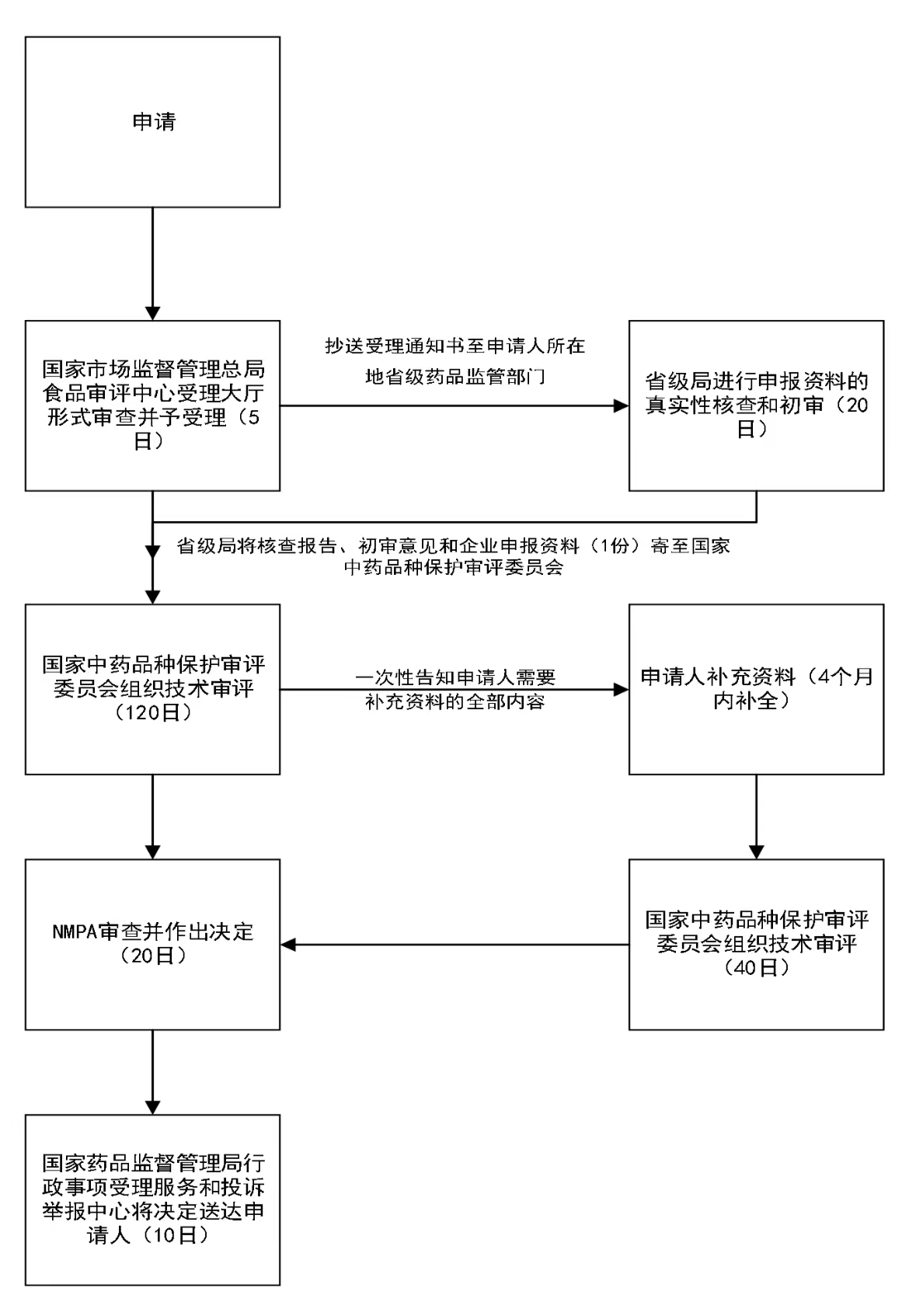
办理流程
流程文字说明
法定办结时限:20个工作日;承诺办结时限:5个工作日
1、受理;
2、初审(必要时组织现场检查);
3、技术评审(国家中药品种保护审评委员会组织专家评审);
4、行政许可决定;
5、送达。
申请材料
1、《中药品种保护申请表》。>>中药品种保护申请表
2、证明性文件:初次保护申请企业应提供其为原研企业的证明资料;现行国家标准、说明书和标签实样;专利权属状态说明书及证明文件。
3、申请保护依据与理由综述。
4、医学相关资料(批准上市前研究资料、批准上市后研究资料)。
5、药学相关资料(批准上市前研究资料、批准上市后研究资料)。
6、药理毒理相关资料(批准上市前研究资料、批准上市后研究资料)。
7、拟改进提高计划与实施方案。
结果样本



常见问题
问题1:什么叫同品种保护申请?
答:同品种是指药品名称、剂型、处方都相同的品种。同品种保护申请是指在首家初次保护申请品种被批准保护(公告)之后,其他同品种生产企业按照《中药品种保护条例》第十八条规定提出的中药品种保护申请。
《中药品种保护条例》第十八条: 国务院药品监督管理部门批准保护的中药品种如果在批准前是由多家企业生产的,其中未申请《中药保护品种证书》的企业应当自公告发布之日起六个月内向国务院药品监督管理部门申报,并依照本条例第十条的规定提供有关资料,由国务院药品监督管理部门指定药品检验机构对该申报品种进行同品种的质量检验。国务院药品监督管理部门根据检验结果,可以采取以下措施:
(一)对达到国家药品标准的,补发《中药保护品种证书》。
(二)对未达到国家药品标准的,依照药品管理的法律、行政法规的规定撤销该中药品种的批准文号。
问题2:同品种保护申请与初次保护申请有何区别?
答:初次保护申请没有申请时限要求,但同品种保护申请必须在首家初次保护申请品种被批准保护(公告)之后的六个月内提出(将申请送达国家市场监督管理总局食品审评中心受理大厅),对逾期申报的不予受理。
初次保护申请品种必须提交完整规范的可保性证明资料,同品种保护申请可以现有的临床试验资料和文献资料按时申报,欠完善的部分在改进提高计划与实施方案中予以明确即可。
问题3:其他没有获得同品种保护的企业,能否继续生产国家中药保护品种?
答:根据《中药品种保护条例》(以下简称《条例》)第十七条的规定,未获得同品种保护的企业应停止该品种的生产,如继续生产,国家药品监督管理局将中止其该品种药品批准文号的效力,并按照《条例》第二十三条的有关规定进行查处。
已受理同品种保护申请的企业,在该品种审评、审批期间可继续生产、销售。
《条例》第十七条:被批准保护的中药品种,在保护期内限于由获得《中药保护品种证书》的企业生产;但是,本条例第十九条另有规定的除外。
《条例》第十九条:对临床用药紧缺的中药保护品种的仿制,须经国务院药品监督管理部门批准并发给批准文号。仿制企业应当付给持有《中药保护品种证书》并转让该中药品种的处方组成、工艺制法的企业合理的使用费,其数额由双方商定;双方不能达成协议的,由国务院药品监督管理部门裁决。
《条例》第二十三条:违反本条例第十七条的规定,擅自仿制中药保护品种的,由县级以上人民政府负责药品监督管理的部门以生产假药依法论处。
伪造《中药品种保护证书》及有关证明文件进行生产、销售的,由县级以上卫生行政部门没收其全部有关药品及违法所得,并可以处以有关药品正品价格三倍以下罚款。
上述行为构成犯罪的,由司法机关依法追究刑事责任。
问题4:申报同品种保护是否有受理时限?
答:有。按照《中药品种保护条例》第十八条的有关要求,应当在首家中药保护品种公告发布之日起六个月内向国家药品监督管理部门申报。对于违反《中药品种保护条例》第十八条规定,无正当理由而逾期不向国家药品监督管理部门申请中药同品种保护而又继续生产同品种中药的,由国家药品监督管理部门中止该中药品种批准文号的效力,同时在国家药品监督管理局网站上公告。
本办事指南摘自药监局官网,如有变动,以官方发布为准。