基本信息
1、办理部门:江苏省药品监督管理局
2、办理方式:网上办理
3、办理地点:南京市建邺区汉中门大街145号江苏省政务服务中心省药监局窗口
4、咨询电话: 12315 CIO咨询:400-003-0818
受理条件
《中华人民共和国行政许可法》第三十二条第五项: 申请事项属于本行政机关职权范围,申请材料齐全、符合法定形式,或者申请人按照本行政机关的要求提交全部补正申请材料的,应当受理行政许可申请。
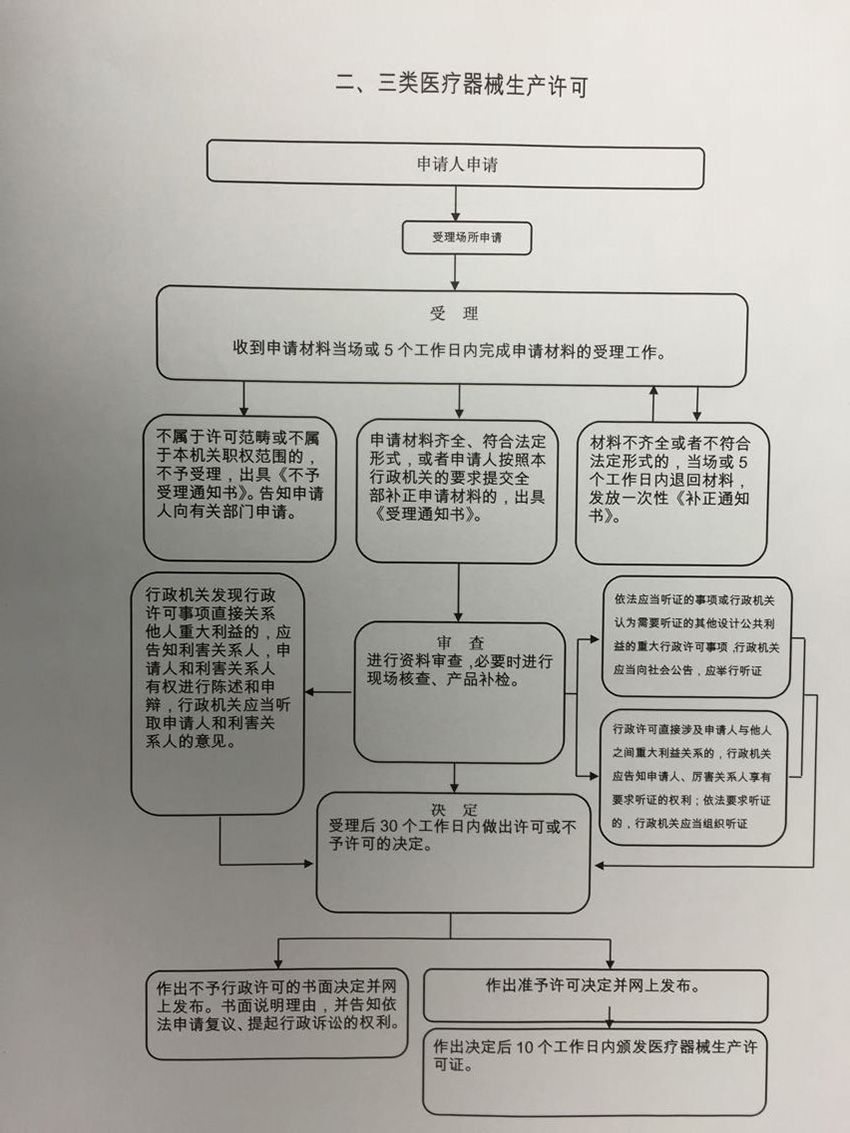
办理流程
流程文字说明
1、审查、决定(时限:20个工作日)
办理结果:根据《医疗器械生产监督管理办法》,对申请材料进行实质内容审查,并做出决定。
申请材料
1、1.医疗器械生产许可事项变更申请表;>>申请表
2、2.变更情况说明(包括变更事项及原因);
3、3.医疗器械生产许可证正本、副本;
4、4.生产场地的相关文件;
5、4.1申请人产权证明、租赁合同复印件;
6、4.2生产地址地理位置图;
7、4.3厂区平面布局;
8、4.4有特殊生产环境要求的,还应当提交设施、环境的相 关文件(如洁净车间平面布局图、新洁净区有资质机构出具的洁净车间环境检验合格报告/原洁净区符合标准要求的最新环境监测合格报告/含全部或部分项目委托有资质机构检测的最新环境监测合格报告、辐射防护证明文件);
9、5.主要生产设备和检验设备目录;
10、5.1主要生产设备器具目录;
11、5.2进货、过程、成品检验设备目录;
12、5.3进货、过程、成品检验规程;
13、6.质量手册和程序文件目录;
14、6.1质量手册和程序文件目录;
15、6.2医疗器械质量管理规范等现场检查申请表;>>核查申请表
16、6.3现场检查的特别说明(如申请部分产品现场考核、书面审核或免于现场考核等情形的理由及证明资料,如适用);
17、6.4现场考核后提交现场检查记录表(含情况说明,如适用);
18、6.5企业整改报告(如适用);
19、6.6复查申请和/或复查报告(如适用);
20、7.产品详细工艺流程图(需注明主要生产方式、外购外协件、关键工序和特殊过程及各工序的生产环境要求);
21、8.新场地所有试生产及检验情况说明(增加生产地址时需提供);
22、9.经办人的授权文件;>>授权委托书
23、10.资料真实性保证声明(含申请企业承诺)。>>承诺书
结果样本

常见问题
问题1:生产企业取得注册证后还需要去补充生产许可证的相关手续吗?
答:生产企业取得了产品注册证后,如果还未取得生产许可证的生产企业,需申请办理医疗器械生产许可证;如果已取得生产许可证的生产企业,办理生产许可变更手续(增加新产品)。
问题2:现有生产许可证在有效期内,新产品取得注册证后,必须要做许可证变更么?
答:生产企业取得新的产品注册证后,必须办理生产许可证变更手续,即增加新产品变更。
本办事指南摘自药监局官网,如有变动,以官方发布为准。