基本信息
1、办理部门:重庆市药品监督管理局
2、办理方式:窗口办理 网上办理 快递申请
3、办理地点:重庆市渝北区宝圣湖街道食品城大道27号重庆市药品监督管理局行政审批服务中心05-09号窗口
4、咨询电话:023-60353664、 023-60353689 CIO咨询:400-003-0818
受理条件
1、药品生产企业需要以第二类精神药品为原料生产普通药品的,应当将年度需求计划报所在地省、自治区、直辖市人民政府药品监督管理部门,并向定点批发企业或者定点生产企业购买。
办理流程
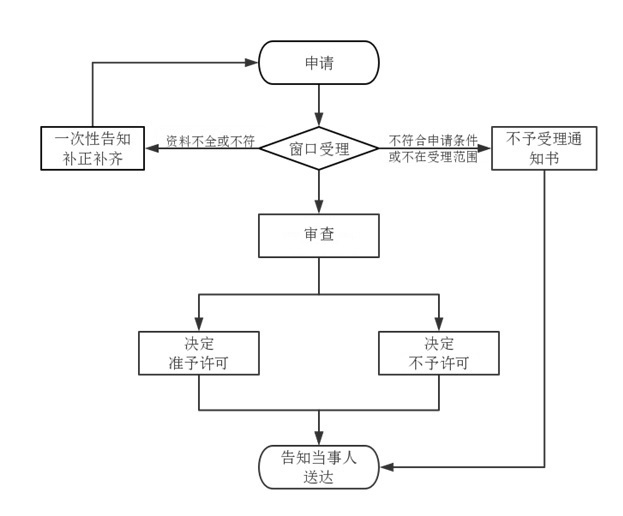
流程文字说明
法定办理时限:20个工作日;承诺办理时限:10个工作日
1、受理(时限:0个工作日)
2、审查(时限:7个工作日)
3、决定(时限:3个工作日)
4、送达(时限:1个工作日)
申请材料
1、工艺设备平面布置图(并注明相应安全管理设施);
2、药品注册批件;
3、法人授权委托书;
4、仓储平面布置图(注明使用、存储麻醉药品和精神药品的位置);
5、企业总平面布置图;
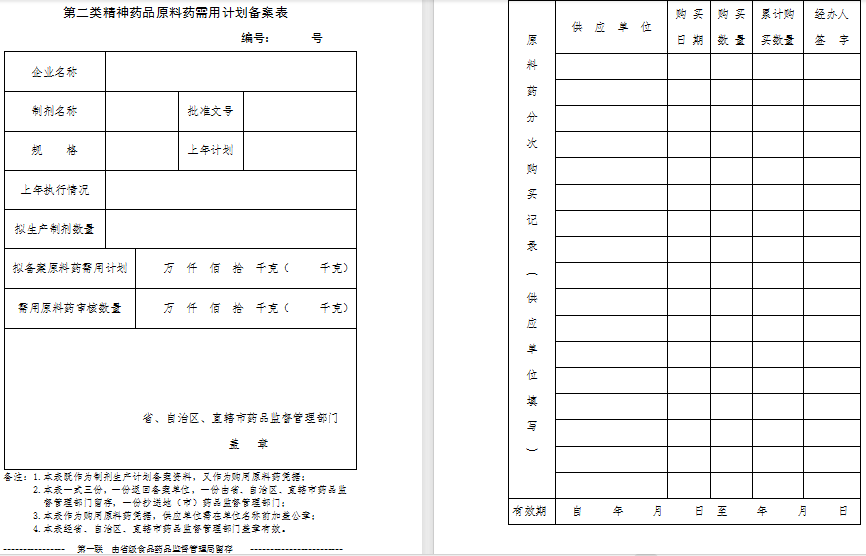
6、第二类精神药品原料药需用计划备案表;
7、申请购买说明文件;
8、企业第二类精神药品管理的组织机构图;
9、第二类精神药品生产工艺布局平面图(非药品生产企业除外);
10、第二类精神药品安全管理制度文件目录;
11、相应剂型符合性检查结果。
结果样本
常见问题
问题1:如需调整本年度需用计划和生产计划,需要重新提出备案申请吗?
答:如需调整本年度需用计划和生产计划,企业应当于每年5月底前向所在地省、自治区、直辖市药品监督管理部门提出备案申请。省、自治区、直辖市药品监督管理部门应当于每年7月20日前签署备案意见。
本办事指南摘自药监局官网,如有变动,以官方发布为准。

























