基本信息
1、办理部门:重庆市药品监督管理局
2、办理方式:窗口办理 网上办理 快递申请
3、办理地点:重庆市渝北区宝圣湖街道食品城大道27号重庆市药品监督管理局行政审批服务中心05-09号窗口
4、咨询电话:023-60353664 CIO咨询:400-003-0818
受理条件
1、按照要求完成IV期临床试验的。
2、未按照规定进行不良反应监测的。
3、在规定时间内提出再注册申请的。
4、按规定履行监测期责任的。
5、无其他不符合有关规定的情形;
6、具备《药品管理法》规定的生产条件的;
7、不属于经国家药监局再评价疗效不确定、不良反应大或者其他原因危害人体健康的;
8、不属于按照《药品管理法》的规定应当撤销药品批准证明文件的;
9、完成国家药品监督管理局批准上市时提出的有关要求的。
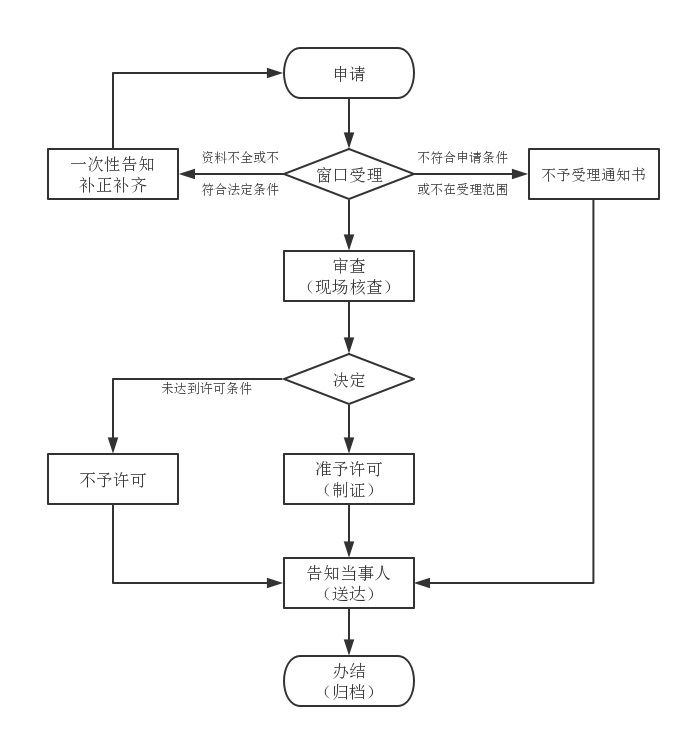
办理流程
流程文字说明
法定办理时限:20个工作日;承诺办理时限:5个工作日
1、受理(时限:0个工作日)
2、审查(时限:8个工作日)
3、决定(时限:1个工作日)
4、颁证(时限:0个工作日)
申请材料
1、境内生产药品再注册申请文件;
2、证明性文件及相关资料;
3、药品上市后评价和不良反应监测情况总结和分析评估情况;
4、按照药品批准证明文件和药品监督管理部门要求开展相关工作的情况说明;
5、药品批准证明文件及其附件载明信息变化情况;
6、药品生产、销售、抽检情况总结;
7、其他。
结果样本

常见问题
问题1:药品再注册什么时候提交申请?
答:按照《药品注册管理办法》的规定,药品批准文号的有效期为5年,有效期届满,申请人应当在有效期届满前6个月申请再注册。
问题2:由谁做出药品不予再注册的决定?
答:经省级药品监督管理部门审查不符合再注册相关规定的,报国家药品监督管理总局,由国家药品监督管理总局进行审查,经审查不符合药品再注册规定的,发出不予再注册的通知,并说明理由。
本办事指南摘自药监局官网,如有变动,以官方发布为准。

























