基本信息
1、办理部门:吉林省药品监督管理局
2、办理方式:窗口办理,网上办理,快递申请
3、办理地点:吉林省长春市南关区人民大街9999号吉林省政务服务中心B1层1-8号综合窗口
4、咨询电话:0431-82752011 CIO咨询:400-003-0818
受理条件
根据《医疗器械生产监督管理办法》 第十条 在境内从事第二类、第三类医疗器械生产的,应当向所在地省、自治区、直辖市药品监督管理部门申请生产许可,并提交下列材料:
(一)所生产的医疗器械注册证以及产品技术要求复印件;
(二)法定代表人(企业负责人)身份证明复印件;
(三)生产、质量和技术负责人的身份、学历、职称相关材料复印件;
(四)生产管理、质量检验岗位从业人员学历、职称一览表;
(五)生产场地的相关文件复印件,有特殊生产环境要求的,还应当提交设施、环境的相关文件复印件;
(六)主要生产设备和检验设备目录;
(七)质量手册和程序文件目录;
(八)生产工艺流程图;
(九)证明售后服务能力的相关材料;
(十)经办人的授权文件。申请人应当确保所提交的材料合法、真实、准确、完整和可追溯。 相关材料可以通过联网核查的,无需申请人提供。 按照“办事指南”提供相关材料。
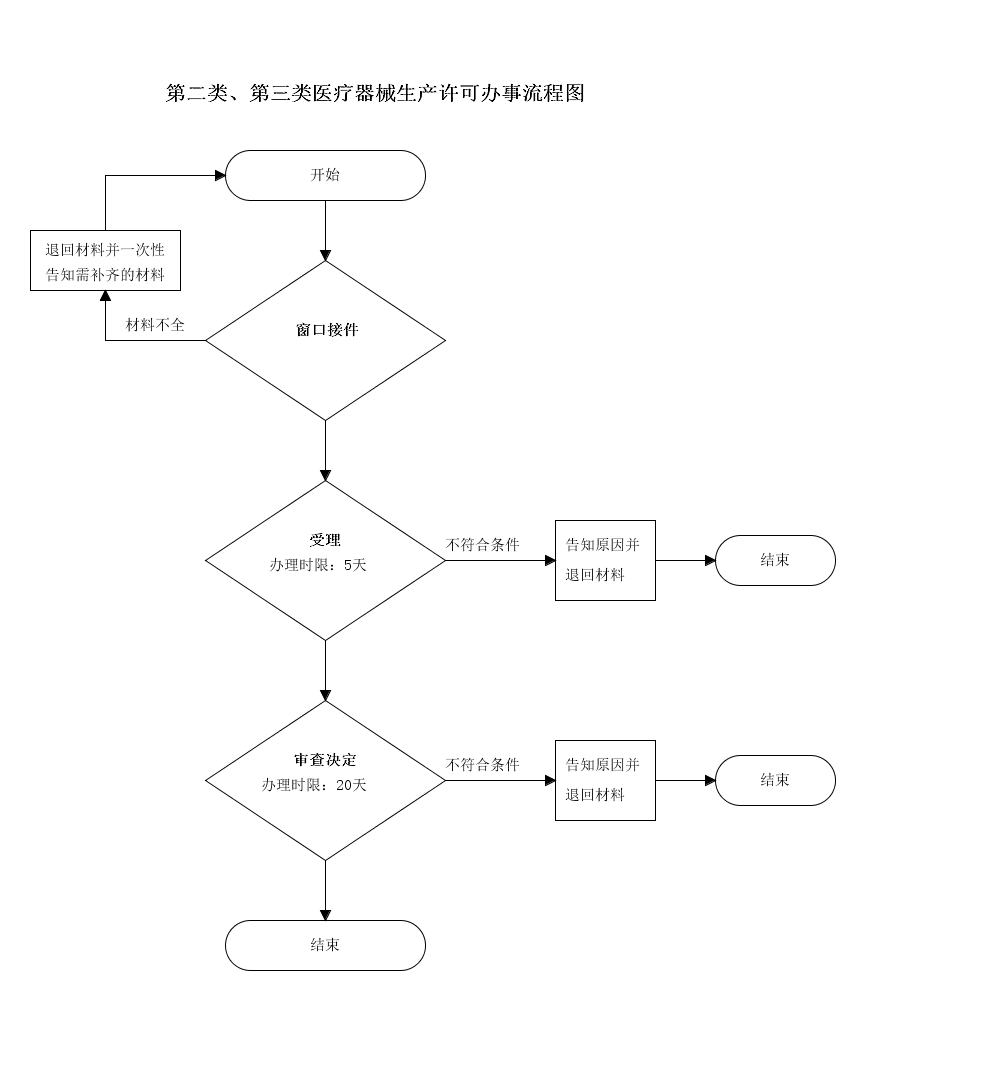
办理流程
流程文字说明
法定办理时限:25个工作日;承诺办理时限:20个工作日
1、受理(时限:5个工作日)
2、审查决定(时限:15个工作日)
申请材料
1、医疗器械生产许可申请表;
2、营业执照;
3、所生产的医疗器械注册证以及产品技术要求复印件;
4、法定代表人(企业负责人)身份证明复印件;
5、生产、质量和技术负责人的身份、学历、职称相关材料复印件;
6、生产管理、质量检验岗位从业人员学历、职称一览表;
7、生产场地的相关文件复印件,有特殊生产环境要求的,还应当提交设施、环境的相关文件复印件;
8、主要生产设备和检验设备目录;
9、质量手册和程序文件目录;
10、生产工艺流程图;
11、证明售后服务能力的相关材料;
12、经办人的授权文件;
13、许可部门要求的其他材料。
结果样本

常见问题
问题1:生产许可证变更与延续能否同时办理?
答:不能,在国家总局系统两项内容不允许同时提交。
问题2:生产许可变更在系统找不到企业资料?
答:需要首先核实企业生产许可开办是否在国家局系统简历基础档案,如若没有需要补录系统,才能进行变更。
本办事指南摘自药监局官网,如有变动,以官方发布为准。
























