基本信息
1、办理部门:吉林省药品监督管理局
2、办理方式:窗口办理,网上办理,快递申请
3、办理地点:吉林省长春市南关区人民大街9999号吉林省政务服务中心B1层1-8号综合窗口
4、咨询电话:0431-82752980 CIO咨询:400-003-0818
受理条件
根据《医疗器械监督管理条例》第二十一条规定及《体外诊断试剂注册与备案管理办法》相关要求,企业填报《体外诊断试剂变更注册申请表》,并按不同情形报送相关材料。要求企业申请材料齐全,符合法定形式;具备法人资格单位。
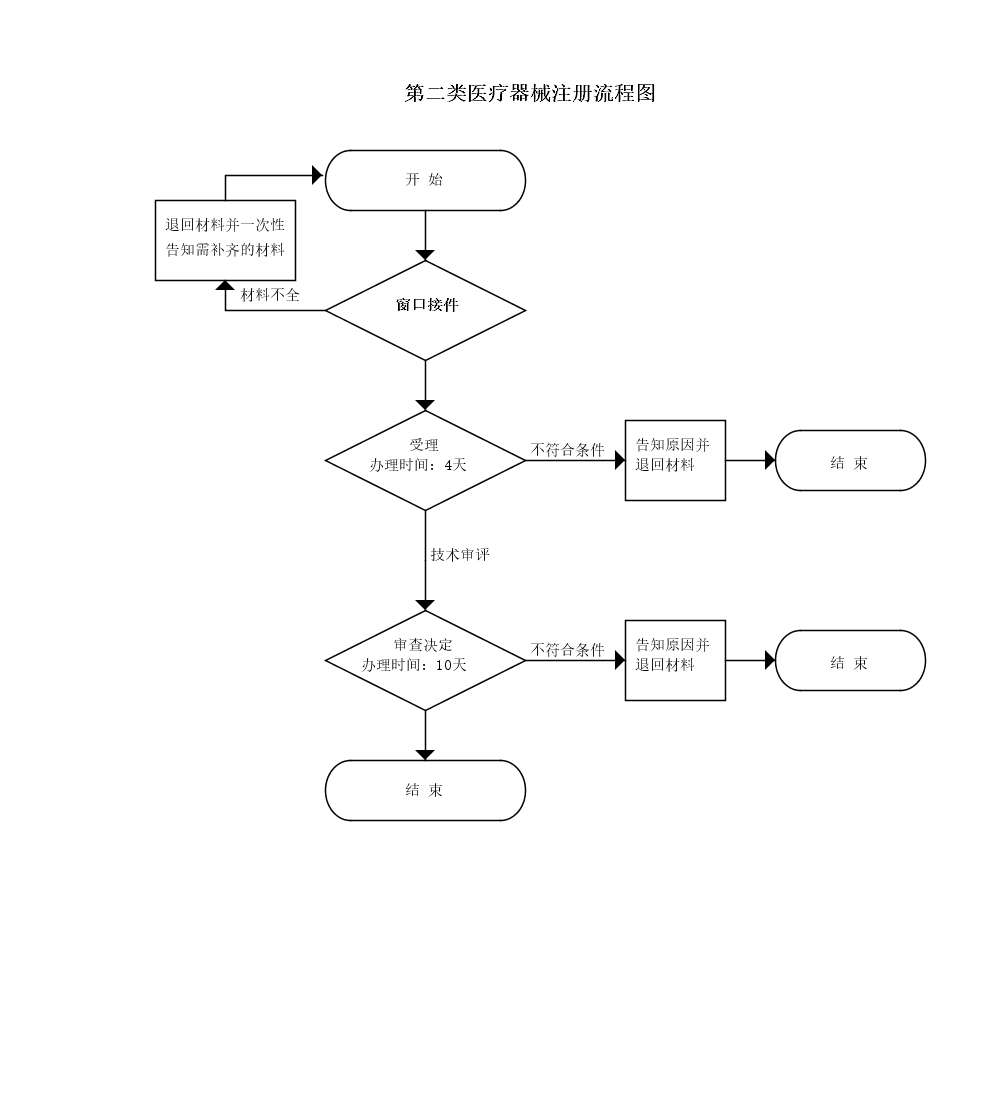
办理流程
流程文字说明
法定办理时限:20个工作日;承诺办理时限:14个工作日
1、受理(时限:4个工作日)
2、技术评审(时限:无)
3、审查决定(时限:10个工作日)
申请材料
情形一:产品名称变化
情形二:包装规格变化
情形三:产品储存条件及有效期变化
情形四:适用仪器变化
情形五:阳性判断值或参考区间变化
情形六:产品技术要求、说明书变化
情形七:适用的样本类型变化
情形八:适用人群变化
情形九:临床适应证变化
情形十:其他可能改变产品安全有效性的变化
1、监管信息-申请表;
2、监管信息-关联文件(注册申请人企业营业执照副本或事业单位法人证书,受托企业营业执照副本、委托生产协议、质量安全协议(如有));
3、监管信息-申报前与监管机构的联系情况和沟通记录;
4、监管信息-符合性声明;
5、综述资料-章节目录;
6、综述资料-概述;
7、非临床资料-产品说明书;
8、综述资料-变更对产品安全性、有效性影响的技术分析;
9、非临床资料-章节目录;
10、非临床资料-产品风险管理资料。
结果样本

常见问题
问题1:行业标准提高修改产品技术要求是否属于许可事项变更,是否收费?
答:行业标准提高企业修改相应技术要求不属于许可事项变更,变更也不收费。
问题2:注册资料格式和内容能否详细说明?
答:详细的填写说明请参照《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》附件4(国家食品药品监督管理总局2014年第43号公告)执行。
本办事指南摘自药监局官网,如有变动,以官方发布为准。
























