 E邀专家
E邀专家
众所周知,一款化妆品质量的好坏,除了配方设计及生产加加工工艺的保证外,还有一个极其重要的因素,就是对于化妆品原料选择。
国家在法规上一直是有着严格的要求,而且在飞行检查及备案工作上,都对化妆品的所使用的组份有着非常严格的要求。 这也恰恰证明对于任何行业来说,安全永远是第一位的。
化妆品这个体现“美”的行业,更加要注意对安全的重视。现在随着国家法规的陆续完善,检查力度的不停加强,如果企业在这个触及红线的事情上,稍有不慎,将会给企业,给社会带来不可估量的影响跟损失。
所以,产品在配方确定前后,在具体需要如何来确定所计划选择的原料是否安全这个问题上,安全性判定这个工作变得非常紧迫跟严肃。争对这个问题,我个人就自已的经验,浅淡一些个人看法。
首先,我们先要调整好自已的心态。之所以这么说,是因为我们化妆品市场从没有规模,到如今的近 3400 亿的市场规模;从当年加工不是非常规范,到如今都在积极在正规化,GMP 管理化;从当初原料采购的松散要求,到如今的严格合法化,其中必有一个心态转换的过程。
所以我们一定要学会做到几下几点:
一是当年只求压低成本的心态,不能再有。
二是要改变对原料来源的模糊审查心态,必须以严谨的心态来对待。
三是企业要努力建成可以对所采购原料进行安全检测的能力。
四是自己有能力的企业,一定要认真检测原料是否达到供方所宣称的内容,如果自身暂不能测试的,但是又存在风险疑虑的原料,则可以让有能力的第三方来做一个测试,并保存好检测结果备查。
在有了这几种好的心态后,接下来的操作会轻忪不少。
首先,原料的采购之前需要认真学习一下几个法规:
第一个是,《化妆品安全技术规范 2015》。这是一个对所使用原料是不是能够达到安全性要求的基本判别标准了,尤其是其中对已经划出了红线1388项化妆品禁用组分,坚决不能出现在你的采购清单中。同时对有使用限制要求的 47 项原料组份,必须慎重选择。
第二个是,国家 2021 年发布的 《已使用化妆品原料目录 2021》,只要不是在这份在目录中出现,但是又没有国家药监局发布的新原料许可的,都不应考虑应用之列。
第三个是,特别要关注你的原料中是不是存在以下 41 种物质:(附表如下)
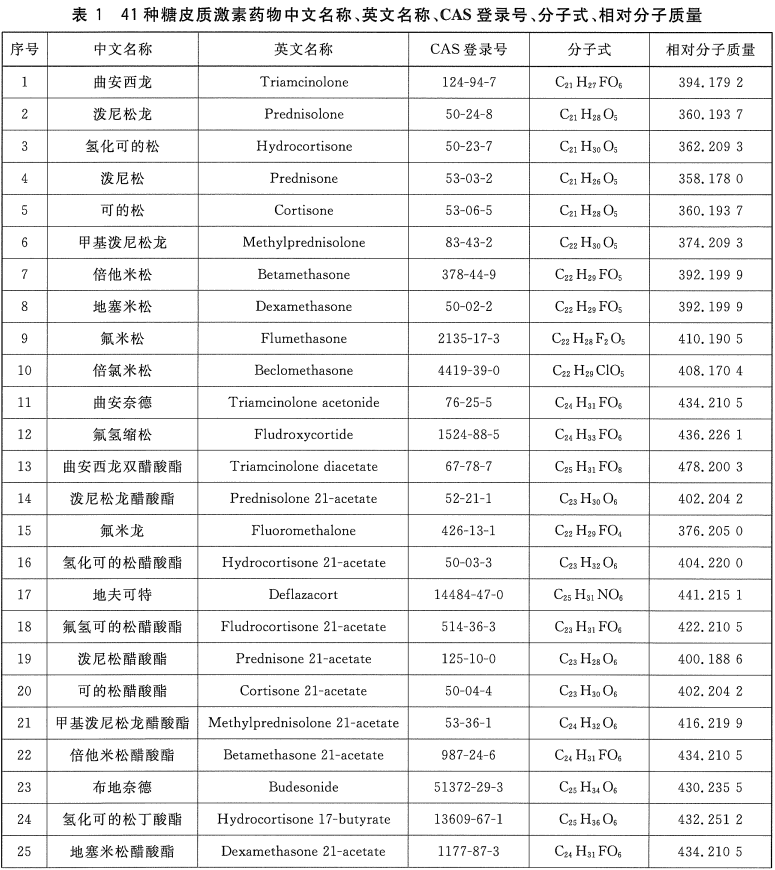
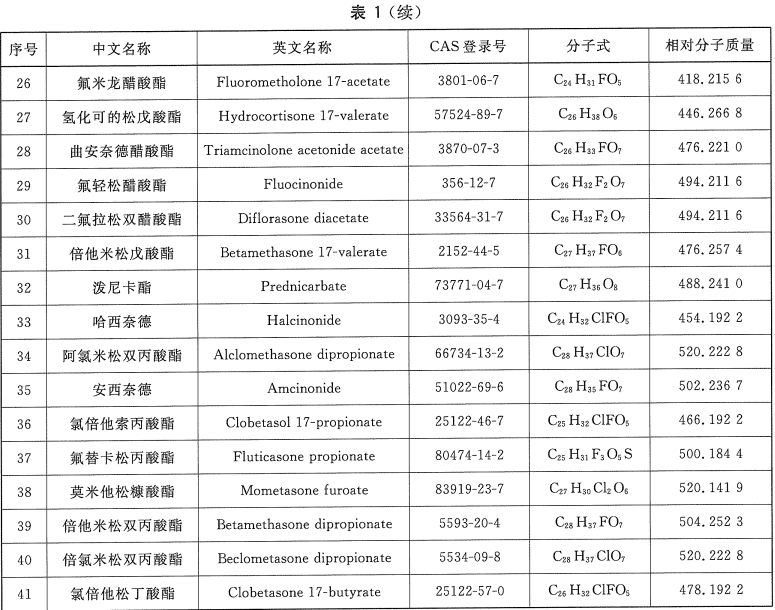
这 41 种具有激素性质的原料组份,要在选择原料时,一定要仔细再仔细,根据目前化妆品抽检出的问题产品,都是因为违规使用这些原料。
明白以上的操作要求后,最后我们来谈谈如何来根据以上的法规要求,来具体判定原料的安全合规性。
第一个是,一定要养成收集需采购原料的 COA 及 MSDS(材料安全数据表)习惯,并仔细去确认所需采购原料的的组份构成,如果在这个 MSDS 中发现有以上不能使用原料或是限组份存在,则必须审惧对待。
第二个是,需要对已使用化妆品原料目录中的原料已使用的最大量进行反复与配方比例确认,再决定是否需要进行采购。
第三个就是在原料采购供应方的选择上,尽量选择品牌强,售后技术实力的供应商,这可以省去不少的后续使用风险产生。
第四个则是需要密切关注一下国家最新的原料使用信息动态,如对《化妆品禁用原料目录》有调整,或是公布哪款原料可以应用于化妆品的最新通知,这样可以非常主动的跟上法规监管要求,不会造成信息闭塞的情况发生。
比如:国家药监局关于更新化妆品禁用原料目录的公告(2021 年第 74 号)调整。
最后,总的来说并不是所有化妆品出现质量问题都是由原料本身所产生,但是做为化妆品生产环节的核心要素,原料的选择是否安合,合法就已决定了这款产品的市场前景。 因此所有的化妆品生产加工企业,都要共同来担负起安全为先这个前提,保证原料合法安全,才会有产品的放心使用。同时,也可以更加从容应对国家的各种检查。
如果您有化妆品注册备案、化妆品原料药报送、化妆品GMP审计需求,点击下方联系我们。
 E邀专家
E邀专家



















