 E邀专家
E邀专家
一、写在前面:为什么这个案例值得分享
在医药合规咨询行业摸爬滚打多年,我经手过不少GMP体系搭建的项目。但去年做的这个细胞治疗企业项目,让我有了一些不一样的感触。
这家企业打动我的地方在于:他们对自己要走的路非常清醒——知道眼下需要什么,也知道未来要面对什么。中试车间是为Ⅱ期临床前准备的,到了Ⅲ期临床和商业化阶段,必须另建符合更大规模生产要求的新场地。他们没有幻想“一步到位”,也没有因为“以后要重建”就对眼前敷衍了事。这种务实和清醒,在行业内并不多见。
企业负责人说的一句话我印象很深:“我们不想走捷径,眼下该做的就做扎实,以后该重建的就重建。每一步都走稳,才能走得远。”
这种态度,让整个合作过程格外顺畅。10个月后,当他们拿到GMP符合性审计证书的那一刻,我由衷为他们感到高兴——不是因为我们又完成了一个项目,而是看到一家真正想做事情的企业,在合规这条路上走对了方向。
下面,我想把这个项目的全过程记录下来,分享给同样在合规路上探索的同行们。
二、项目背景:一家想“走稳每一步”的细胞治疗企业
2024年底,一家位于长三角的细胞治疗研发企业找到了我们。经过几个月的接洽、现场考察、方案评估,该企业最终决定选择与CIO合作。
在找到我们之前,他们对“质量管理体系”的接触,主要来自几年前做过的一次ISO认证。那次认证让他们有了一些基础的体系认知,比如文件控制、内部审核、管理评审等概念。但企业负责人也坦诚,那次认证主要是为了满足客户和市场的需求,通过之后体系并没有真正融入日常运营。后来缺乏体系的日常维护,最终没法通过后续的年度监督检查。
这家公司专注于靶向细胞治疗产品的研发,核心产品包括靶向树突细胞疫苗等。企业已完成早期研发,正准备进入中试放大阶段。他们对自己的定位非常清晰:
现有场地:中试车间,服务于Ⅱ期临床前研究
未来规划:Ⅲ期临床及商业化生产需要新建符合更大规模的生产场地
眼下任务:把中试车间的GMP体系做扎实,确保Ⅱ期临床前的样品质量可靠、数据完整。
企业负责人的原话是:“我们现在这个车间,就是为Ⅱ期临床前服务的。以后到了Ⅲ期,肯定要重建。但眼下的事必须做好,不能因为以后要重建,现在就糊弄。每一步都算数。”
这种清醒的认知,让我们对这个项目充满信心。
客户核心诉求:
短期目标:向医疗机构申请ⅡT(研究者发起的临床研究),需要证明样品在符合GMP条件下生产。
中期目标:为未来Ⅱ期临床前试验提供质量可靠的样品。
长期规划:未来Ⅲ期临床及商业化生产将新建场地,眼下不做过度投资。
三、破局思路:把眼下的事做扎实,不为未来过度设计
项目于2025年3月正式启动。在项目启动前的沟通中,我们项目团队反复讨论一个问题:对于“已知将来要重建”的中试车间,我们应该怎么做?
最终确定了三条原则:
第一,不做过度设计。不要求这个车间2019年就建成的车间去满足Ⅲ期临床和商业化的产能需求,那些是未来新建场地要考虑的事。我们就按照Ⅱ期临床前的要求,把该做的做到位。
第二,但也不能“减配”。Ⅱ期临床前的GMP要求一点都不能打折扣——无菌模拟试验、工艺验证、偏差管理、变更控制,该做的全都要做,而且要做扎实。因为样品质量直接关系到临床试验结果,容不得半点马虎。
第三,体系要有“可移植性”。虽然现在这个车间以后要淘汰,但今天建立的文件体系、验证方法、人员能力,未来可以平移到新场地。这样今天的投入,到了明天依然是资产,不是沉没成本。
带着这些想法,我们制定了“体系建设+硬件完善+人员赋能+验证先行”的整体策略。
项目目标:在10个月内,帮助企业建立完善的GMP体系,顺利通过GMP符合性审计,获得可支持Ⅱ期临床前的GMP符合性审计证书。
四、服务过程:一步步见证体系的生长
第一步:差距分析——找到起点(2025年3月)
项目启动后,我们组织专家团队第一时间去了企业现场,对车间的硬件条件、文件体系、人员能力、验证状态等进行了全面评估。
我们把这些发现整理成了一份 《GMP差距分析报告》 ,列出了需要改进的关键事项,并按优先级分了类。企业看到报告后说:“这下心里有数了,知道从哪里下手了。”
第二步:硬件确认与管理完善(2025年4月-6月)
针对硬件方面的情况,我们采取的策略是:不盲目追求大规模改造,而是通过系统性的验证、严格的管理制度和风险防控措施,确保现有条件下能够满足Ⅱ期临床前的生产要求。
主要工作包括:
Ø 指导对洁净空调系统、压差梯度、关键设备进行全面的验证和确认;
Ø 指导建立连续环境监测体系,明确监测点位、频率、警戒限和行动;
Ø 完善人员行为规范,确保操作本身不成为污染源。
通过上述工作,确保了现有条件下能够满足生产要求。
第二步:体系完善与人员赋能(2025年4月-10月)
体系建设的这几个月,是工作量最大的阶段,也是最有成就感的阶段。
文件体系方面,我们不是简单给一套模板让他们填空,而是带着企业的人一起写。我常说:“文件要写得让操作的人看得懂、做得到。”比如细胞培养的SOP,我们让负责操作的实验员参与编写,他们最清楚哪个步骤容易出错、哪个环节需要特别注意。最后定稿的文件,既符合GMP要求,又贴合实际。
到10月份,企业建立了完善的文件体系,覆盖了所有关键环节,包括管理规程(SMP)、操作规程(SOP)、技术标准、记录表格等三百多份文件。
人员培训方面,我们坚持“培训+考核+再培训”的闭环管理。培训内容覆盖了GMP法规通识、细胞治疗附录专项、无菌操作规范、偏差管理、变更控制等。
更让人欣慰的是,操作人员开始主动提问:“老师,如果遇到偏差,第一步应该是先停还是先报?”这种从“被动执行”到“主动思考”的转变,正是GMP意识内化的表现。
第四步:无菌模拟试验(2025年11月)
无菌模拟试验(APS)是细胞治疗产品GMP验证的重头戏。连续3批全部合格,才能证明无菌操作工艺有效。
说实话,做APS的那段时间,企业上下都绷着一根弦。每批试验结束后的7天、14天,每天观察培养结果时的紧张感,我们能真切感受到。
好在结果是让人欣慰的:连续3批无菌模拟试验全部合格。那一刻,所有人都松了口气。这不仅是对无菌操作工艺的验证,更是对团队几个月来努力的肯定。
与此同时,清洁验证、分析方法验证、运输验证等工作也同步推进。到10月份,全套验证文件归档完成,为后续的样品生产提供了充分的数据支持。
第五步:工艺验证(2025年12月)
在无菌模拟试验合格的基础上,企业启动了工艺验证工作。核心产品完成了连续3批工艺验证,每一批的数据都经得起推敲。
第六步:自查整改(2025年12月-1月)
正式审计前,企业开展了多轮自查。我们带着团队又去了两次,做模拟检查。
模拟检查的时候,我们尽量模拟真实审计的场景:随机抽文件、现场看操作、随机提问。这种“实战演练”让团队提前进入了状态,也把问题解决在了正式审计之前。
经过几轮自查和整改,所有发现的问题都关闭了。这时候,企业才向审计机构提交了正式申请。
第七步:GMP符合性审计与整改辅导(2026年2月)
2026年2月,GMP审计首次会议召开。企业的汇报材料准备得很充分,从企业概况、产品研制、GMP体系建立执行,到自查整改情况,条理清晰,数据详实。
正式审计持续了2天。审计专家们看得很细:文件、记录、现场、人员,每个环节都不放过。
审计结束后,专家组出具了正式的《GMP审计报告》,列出了需要整改的缺陷项。 虽然整体体系得到了认可,但任何审计都会发现一些需要完善的地方——这是正常的,也是GMP持续改进精神的体现。
接下来的半个月,是整改辅导阶段。我们协助企业对每一条缺陷项进行分析:
对于文件类缺陷:指导如何修订文件,使其更清晰、更具可操作性
对于记录类缺陷:帮助完善记录设计,确保数据完整性;
对于现场类缺陷:协助制定整改方案,明确责任人和完成时限
对于验证类缺陷:指导补充验证工作,确保数据充分;
每周一次的进度跟踪,确保整改按计划推进。所有整改完成后,我们辅导企业撰写了整改报告,附上整改前后的对比证据,提交给审计机构复核。
2026年2月,企业正式收到了GMP符合性审计证书(证书样本详见附件)。
五、项目成果与客户价值
回看这10个月,最大的成就感不是那张证书,而是看到企业真正建立起了一套“活的体系”:
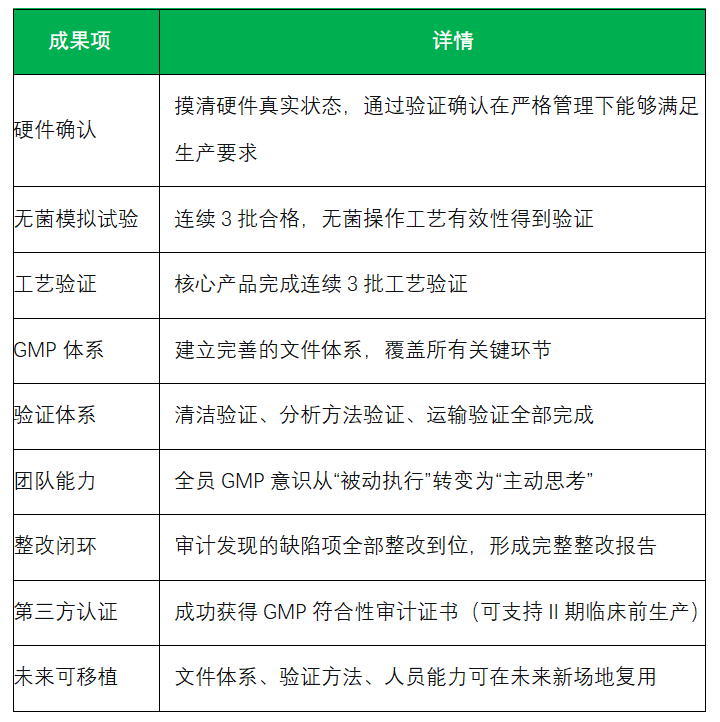
六、一点感想
写完这个案例,我想到那些和这家企业处境相似的客户——硬件条件不完美,但又必须推进GMP合规。他们常常问我:“像我们这种情况,还有机会通过审计吗?”
我的回答是:有机会,但有前提。
前提是:你清楚地知道这个场地是过渡还是永久;你愿意在管理和验证上下硬功夫,而不是指望侥幸过关;你有充分的数据证明风险可控,而不是凭感觉说“我觉得没问题”。
就像这家企业,他们从没幻想过用这个中试车间去走完Ⅲ期临床。他们知道,未来一定要建新场地。但他们同样清楚,今天的样品质量,直接关系到明天的临床试验结果。所以,该做的无菌模拟试验,他们做了;该做的工艺验证,他们做了;该写的SOP,他们一条一条写;该培训的人员,他们一个一个考。
最后能拿到证书,不是因为硬件有多完美,而是因为他们在现有条件下,把能做的事都做到了极致。
如果你也在类似的路上,希望这个案例能给你一些参考。
附件:GMP符合性审计证书样本

 E邀专家
E邀专家
最新推荐
热门观点

合规营销体系搭建

药械企业法律风险预防与应对系列培训

药品上市后临床评价・真实世界研究 & 药物警戒全链条服务

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务

生死红线——「医改+反腐」背景下的医药企业生存逻辑与增长路径企业内训

药品医疗器械企业安全风险排查服务

【医药传播】药企品牌 / 产品宣传片制作

医疗器械注册/备案、变更

药品(国产/进口)注册、变更

药品经营许可申请 / 变更

化妆品生产许可申请/变更

医疗器械生产许可申请/变更

药品上市许可持有人的B证申请

药品生产许可申请 / 变更(药厂筹建)

原辅包注册/登记

化妆品注册/备案、变更

合规营销体系搭建

药械企业法律风险预防与应对系列培训

药品上市后临床评价・真实世界研究 & 药物警戒全链条服务

执业药师继教服务

合规破局与价值重塑 医药营销转型实战训练营

药物警戒第三方委托服务





