浙江省药品监督管理局关于国家药品监督管理局批准注册第三类医疗器械产品通告(2024第3号)
行政许可 产品 浙江省
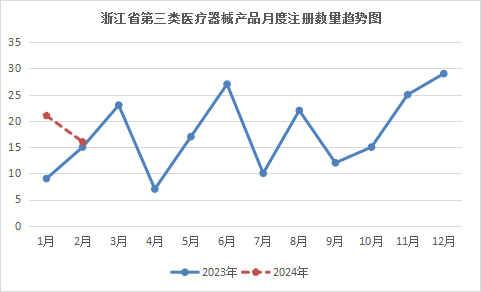
根据国家药品监督管理局2024年第23号公告,2024年2月,国家药品监督管理局共批准注册境内第三类医疗器械产品148个。
我省医疗器械生产企业获得国家局批准注册第三类医疗器械产品16个,其中有源产品4个,无源产品5个,体外诊断试剂7个,占境内第三类医疗器械产品注册总数的10.81%。按生产企业所在辖区分,杭州市6个,嘉兴市1个,台州市2个,宁波市7个(具体产品见附件)。
特此通告。
浙江省药品监督管理局
2024年3月13日
2024年2月国家药品监督管理局批准注册浙江省第三类医疗器械产品目录
序号 | 产品名称 | 注册人名称 | 注册证编号 | 产品类型 | 所在辖区 |
境内第三类医疗器械 | |||||
1 | 乙型肝炎病毒e抗原检测试剂盒 (化学发光免疫分析法) | 美康生物科技股份有限公司 | 国械注准20243400258 | IVD | 宁波 |
2 | 乙型肝炎病毒e抗体检测试剂盒 (化学发光免疫分析法) | 美康生物科技股份有限公司 | 国械注准20243400261 | IVD | 宁波 |
3 | 甲型/乙型流感及呼吸道合胞病毒核酸联合检测试剂盒 (实时荧光PCR法) | 嘉兴市艾科诺生物科技有限公司 | 国械注准20243400263 | IVD | 嘉兴 |
4 | 持续葡萄糖监测系统 | 微泰医疗器械(杭州)股份有限公司 | 国械注准20243070269 | 有源 | 杭州 |
5 | 一次性使用精密过滤输液器 带针 | 浙江康康医疗器械股份有限公司 | 国械注准20243140280 | 无源 | 台州 |
6 | 人类免疫缺陷病毒抗原抗体检测 试剂盒(化学发光免疫分析法) | 美康生物科技股份有限公司 | 国械注准20243400289 | IVD | 宁波 |
7 | 聚醚醚酮带线锚钉 | 宁波五洲医疗器械有限公司 | 国械注准20243130299 | 无源 | 宁波 |
8 | 颅内球囊扩张导管 | 浙江归创医疗科技有限公司 | 国械注准20243030312 | 无源 | 杭州 |
9 | 一次性使用透析用留置针 | 宁波百通医疗科技有限公司 | 国械注准20243100322 | 无源 | 宁波 |
10 | 冠状动脉球囊扩张导管 | 浙江桐轩医疗科技有限公司 | 国械注准20243030323 | 无源 | 台州 |
11 | 新型冠状病毒2019-nCoV核酸检测试剂盒(PCR荧光探针法) | 宁波海尔施基因科技股份有限公司 | 国械注准20243400354 | IVD | 宁波 |
12 | X射线骨龄仪 | 杭州沧澜医疗科技有限公司 | 国械注准20243060357 | 有源 | 杭州 |
13 | X射线计算机体层摄影设备 | 明峰医疗系统股份有限公司 | 国械注准20243060360 | 有源 | 杭州 |
14 | 乙型肝炎病毒表面抗体检测试剂盒(化学发光免疫分析法) | 美康生物科技股份有限公司 | 国械注准20243400368 | IVD | 宁波 |
15 | 等离子手术设备 | 杭州超凯医疗科技有限公司 | 国械注准20243010376 | 有源 | 杭州 |
16 | 幽门螺杆菌IgG抗体检测试剂 (荧光免疫分析法) | 艾康生物技术(杭州)有限公司 | 国械注准20243400380 | IVD | 杭州 |
相关推荐
CIO提供以下相关文库下载、合规服务以及线上培训课程学习。


















