中国医疗器械标准管理年报(2023年度)
药监头条 全国
2023年是全面贯彻党的二十大精神的开局之年,国家药监局坚持以习近平新时代中国特色社会主义思想为指导,严格践行“最严谨的标准”要求,深入落实《国家标准化发展纲要》《“十四五”国家药品安全及促进高质量发展规划》,不断加快构建推动高质量发展的标准体系,着力提升医疗器械标准支撑科学监管、助力高技术创新、促进高水平开放、引领高质量发展的积极作用。
一、医疗器械标准数据概览
(一)医疗器械标准制修订计划下达数据
1.国家标准制修订计划。2023年,国家标准委批准下达医疗器械国家标准立项计划52项,按照标准制修订划分,制定34项(占比65.4%),修订18项(占比34.6%);按照标准性质划分,强制性标准计划4项(占比7.7%),推荐性标准计划46项(占比88.5%),指导性技术文件2项(占比3.8%)。
2.行业标准制修订计划。2023年,国家药监局批准下达医疗器械行业标准立项计划117项,按照标准制修订划分,制定57项(占比48.7%),修订60项(占比51.3%);按照标准性质划分,强制性标准计划15项(占比12.8%),推荐性标准计划102项(占比87.2%),其中企业牵头标准项目22项(占比18.8%)。
(二)医疗器械标准批准发布数据
1.国家标准。2023年,国家标准委批准发布医疗器械国家标准28项,按照标准制修订划分,制定13项(占比46.4%),修订15项(占比53.6%);按照标准性质划分,强制性标准5项(占比17.9%),推荐性标准21项(占比75.0%),指导性技术文件2项(占比7.1%)。
2.行业标准。国家药监局批准发布医疗器械行业标准131项,按照标准制修订划分,制定68项(占比51.9%),修订63项(占比48.1%);按照标准性质划分,强制性标准33项(占比25.2%),推荐性标准98项(占比74.8%)。发布医疗器械行业标准修改单14项。
(三)现行医疗器械标准数据
1.标准总体数据
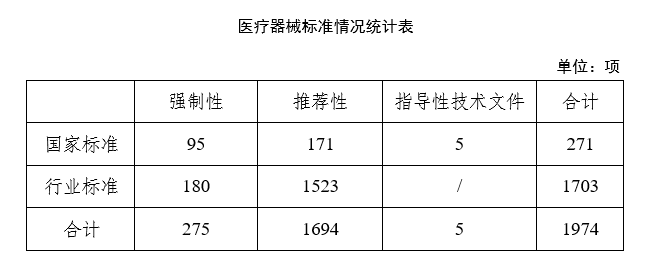
截至2023年12月31日,现行有效医疗器械标准共计1974项,其中国家标准271项,行业标准1703项(见下表)。
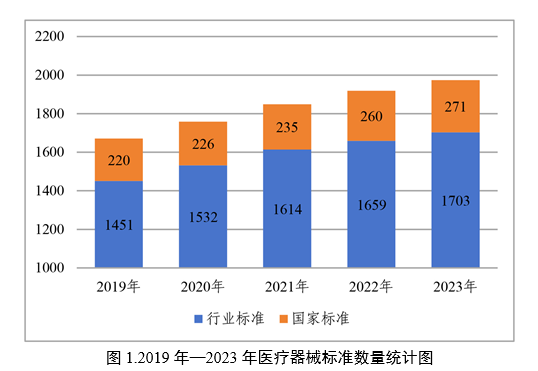
2019年—2023年,国家标准和行业标准数量呈现逐年稳定上升趋势(见图1)。
2.标准分类数据
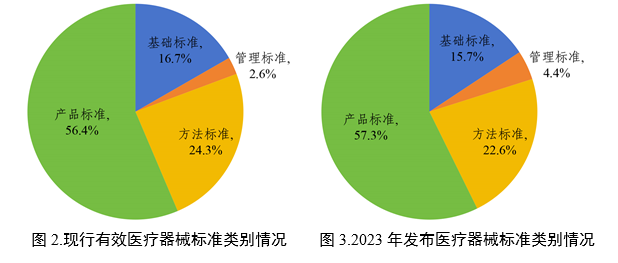
按标准规范对象统计,现行有效的医疗器械标准中基础标准330项,占比16.7%;管理标准51项,占比2.6%;方法标准480项,占比24.3%;产品标准1113项,占比56.4%(见图2)。2023年发布基础标准25项,占比15.7%;管理标准7项,占比4.4%;方法标准36项,占比22.6%;产品标准91项,占比57.3%(见图3)。
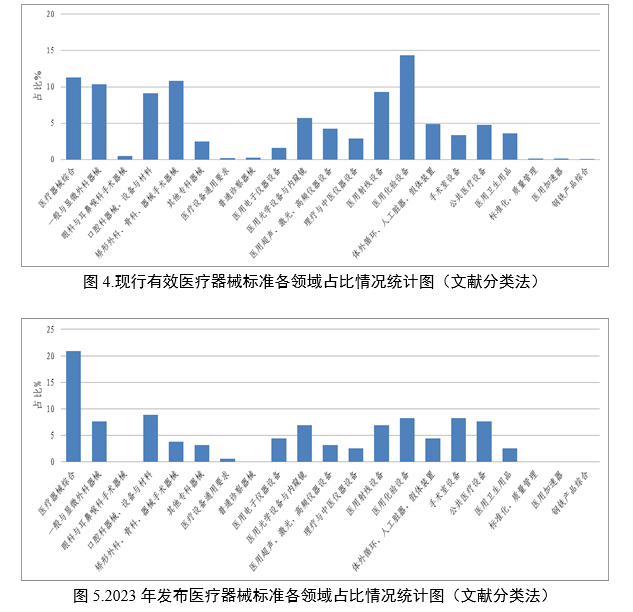
按《中国标准文献分类法》分类统计,现行有效的医疗器械标准全面覆盖了医疗器械各技术领域,主要集中在医用化验设备C44(占比14.3%),医疗器械综合C30(占比11.3%),矫形外科、骨科器械C35(占比10.8%),一般与显微外科器械C31(占比10.4%);2023年发布标准覆盖医疗器械综合C30、口腔科器械、设备与材料C33等16个标准类别,医疗器械综合类标准发布数量最多,占比达到当年发布标准的20.9%。各领域标准占比分布见图4—5。
(四)标准技术组织机构数据
2023年,国家标准委成立全国医用防护器械标准化工作组(SAC/SWG30),国家药监局批准成立医疗器械可靠性与维修性标准化技术归口单位(SMD/TU009)和口腔数字化医疗器械标准化技术归口单位(SMD/TU010),批准筹建医疗器械包装标准化技术归口单位。截至2023年12月31日,医疗器械标准技术组织共计38个,包括13个总标委会(TC)、13个分标委会(SC)、2个标准化工作组和10个技术归口单位(见图6)。

二、医疗器械标准重点工作
(一)标准制度体系固本夯基
2023年国家药监局修订发布《医疗器械标准报批发布工作细则》,进一步规范医疗器械标准报批发布;组织器械标管中心制定印发《医疗器械国家标准和行业标准确定原则》《医疗器械强制性标准确定原则》,厘清标准层级和范围;制定印发《医疗器械标准实施评价工作细则》《医疗器械标准意见反馈及处理机制》,解决标准实施“最后一公里”问题;印发《企业牵头起草医疗器械推荐性行业标准工作规范(试行)》,明确企业牵头标准制修订职责要求,推动医疗器械高质量发展的标准制度体系进一步健全。
(二)构建标准组织体系立体支撑结构
根据国际标准化组织对口情况,组织全国医疗器械质量管理和通用要求标准化技术委员会组建医疗器械液体和气体用小孔径及贮液容器输送系统用连接件工作组,组织全国外科植入物和矫形器械标准化技术委员会组建增材制造植入器械标准工作组、植入陶瓷材料标准工作组、植入金属材料标准工作组、植入高分子材料标准工作组等4个工作组,基本构建起横向(总标委、工作组、归口单位)到边,纵向(分标委)到底,垂直(标委会直属工作组)支撑的医疗器械标准组织体系立体架构。
(三)做好新阶段疫情防控标准技术储备
2023年,密切关注猴痘病毒防控情况,组织提出《猴痘病毒核酸检测试剂盒质量评价要求》国家标准立项申请,规范猴痘病毒核酸检测试剂盒的生产和质量控制;组织开展《新型冠状病毒核酸检测试剂盒质量评价要求》《新型冠状病毒抗体检测试剂盒质量评价要求》《新型冠状病毒IgG抗体检测试剂盒质量评价要求》《新型冠状病毒抗原检测试剂盒质量评价要求》《新型冠状病毒IgM抗体检测试剂盒质量评价要求》等5项国家标准外文版翻译,为我国新冠疫情防控转段储备坚实技术基础。
(四)全面完成标委会双覆盖考核评估
为进一步加强和规范标委会管理,组织完成对象范围和指标内容双覆盖的标委会考核评估工作。考评范围上全覆盖了2020年1月1日前成立并在考核年度内已开展标准化工作的32个标委会,考核指标内容上全覆盖了考核年度内标委会标准管理和报批标准质量。严格按照考核评估细则要求,采用专家审核和交叉互审方式对标委会2021—2022年度标准化工作进行全要素、全内容、全链条评估,量化考核指标,通报考核结果,直击问题、直面难点,补缺补漏、破解难题,通过强化“硬约束”提升“软实力”。
(五)企业牵头行业标准制修订接续发力
为充分发挥企业在标准制修订中的主体作用,鼓励以企业为主体牵头起草医疗器械行业标准的积极性,2022年国家药监局试点面向社会公开征集6项医疗器械标准第一起草单位,探索建立企业牵头起草推荐性行业标准工作机制。2023年《企业牵头起草医疗器械推荐性行业标准工作规范(试行)》印发,并下达22项企业牵头标准制修订工作任务,企业牵头、标委会指导的工作模式初步确立,企业牵头起草行业标准从先行先试逐步向示范引领过渡。
(六)规范推进标准复审和实施评价
规范开展标准复审和标准实施评价工作是提高标准质量,保证标准有效性、先进性和适用性的重要手段。2023年国家药监局进一步强化标准复审工作要求,并加快推进标准实施评价体系建设。完成942项现行医疗器械标准复审,提出复审结论;组织开展45项典型标准实施评价,形成实施评价工作报告。2023年8月,山东省医疗器械和药品包装检验研究院和湖北省医疗器械质量监督检验研究院成功获批首批国家强制性标准实施情况统计分析点(医疗器械),统计分析点将对重点领域强制性国家标准实施全过程进行监测和评估,建立科学、准确、全面的实施评价体系,助力医疗器械标准质量再升级。
(七)建立与国际标准快速联动的标准更新机制
我国医疗器械标准化工作始终坚持“立足国情、面向国际、对标先进”的工作目标,对符合我国国情适合转化的国际标准,密切跟踪,提前研究,同步转化,原则上国际标准发布2年内转化。2023年已发布医疗器械国家、行业标准中采用国际标准的共66项,86项医疗器械国际标准转化为我国国家标准或行业标准的立项计划已批准下达,医疗器械国际标准一致性程度达90%以上。
(八)医疗器械标准国际化进程加快
2023年我国主导制定的国际标准《输液器具进气器件气溶胶细菌截留试验方法》(标准号ISO 24072:2023)正式发布,国际标准提案《人工智能医疗器械肺部影像辅助分析软件算法性能测试方法》(项目号IEC 63524 ED1)成功立项,6项国际标准制修订和9项医疗器械外文版标准转化工作稳步推进,推荐2名中国专家成功当选IEC SC 62B主席和IEC TC62副主席,组织参加国际标准会议共52次,代表我国参与对口国际标准化组织的国际标准投票129次,新增国际标准化组织注册专家8人,医疗器械标准国际化从融入走向融合。
(九)积极营造标准化良好社会氛围
2023年成功举办第54届“标定创新械助健康”世界标准日主题宣传活动,组织开展咨询日、座谈会、主题演讲、标准进企业等多种形式的活动,广泛在全社会宣传、推广、普及标准化理念,凝聚标准化共识;同时,组织举办医疗器械标准综合知识培训班和标准工作专题交流汇报会,宣讲标准化法规政策,分享标准化工作经验;印制2期《医疗器械标准科学与研究》内部交流材料,为医疗器械标准科研和学术交流搭建便捷平台。
(十)标准服务理念一以贯之
标准的生命在于实施。医疗器械标准化工作始终秉承服务理念,持续加大标准公开力度保障标准可及性,加强标准培训引导标准规范使用,推动标准有效实施。2023年公开标准草案征求意见179项,公开全部强制性医疗器械行业标准和非采标推荐性行业标准文本1283项,公开2023版《医疗器械标准目录》,开设医疗器械标准培训和解读专栏,公开医疗器械标准解读140项,公开已发布75项新版GB 9706系列标准培训视频,浏览量超150万次,组织宣贯培训医疗器械标准203项,其中新版GB 9706标准公益培训班,参训千余人。
2023年发布的医疗器械国家标准清单
序号 | 标准编号 | 标准名称 | 发布日期 | 实施日期 | 归口单位 | 发布公告 |
1 | GB/T 13797—2023 | 医用X射线管通用技术条件 | 2023/3/17 | 2024/4/1 | 全国医用电器标准化技术委员会医用X射线设备及用具分技术委员会 | 2023年第1号 |
2 | GB/T 19973.1—2023 | 医疗保健产品灭菌 微生物学方法 第1部分:产品上微生物总数的确定 | 2023/3/17 | 2024/10/1 | 全国消毒技术与设备 | 2023年第1号 |
3 | GB/T 11748—2023 | 激光治疗设备 二氧化碳激光治疗机 | 2023/5/23 | 2024/6/1 | 国家药品监督管理局 | 2023年第2号 |
4 | GB/T 12257—2023 | 激光治疗设备 氦氖激光治疗机 | 2023/5/23 | 2024/6/1 | 国家药品监督管理局 | 2023年第2号 |
5 | GB/T 11417.8—2023 | 眼科光学 接触镜 第8部分:有效期的确定 | 2023/9/7 | 2024/10/1 | 国家药品监督管理局 | 2023年第9号 |
6 | GB/T 28538—2023 | 眼科光学 接触镜和接触镜护理产品 兔眼相容性研究试验 | 2023/9/7 | 2024/10/1 | 国家药品监督管理局 | 2023年第9号 |
7 | GB/T 28539—2023 | 眼科光学 接触镜和接触镜护理产品 防腐剂摄入和释放的测定 | 2023/9/7 | 2024/10/1 | 国家药品监督管理局 | 2023年第9号 |
8 | GB/T 42984.1—2023 | 健康软件 第1部分:产品安全的通用要求 | 2023/9/7 | 2024/10/1 | 全国医用电器标准化 | 2023年第9号 |
9 | GB/T 43050—2023 | 血液透析和相关治疗用液体的制备和质量管理 通用 | 2023/9/7 | 2025/4/1 | 全国医用体外循环设备标准化技术委员会 | 2023年第9号 |
10 | GB 8599—2023 | 大型压力蒸汽灭菌器技术 | 2023/9/8 | 2026/10/1 | 国家药品监督管理局 | 2023年第10号 |
11 | GB 18279—2023 | 医疗保健产品灭菌 环氧乙烷 医疗器械灭菌过程的开发、确认和常规控制要求 | 2023/9/8 | 2026/10/1 | 国家药品监督管理局 | 2023年第10号 |
12 | GB 4234.9—2023 | 外科植入物 金属材料 第9部分:锻造高氮不锈钢 | 2023/11/27 | 2025/12/1 | 国家药品监督管理局 | 2023年第12号 |
13 | GB 19082—2023 | 医用一次性防护服 | 2023/11/27 | 2025/12/1 | 国家药品监督管理局 | 2023年第12号 |
14 | GB 19083—2023 | 医用防护口罩 | 2023/11/27 | 2025/12/1 | 国家药品监督管理局 | 2023年第12号 |
15 | GB/T 16886.12—2023 | 医疗器械生物学评价 第12部分:样品制备与参照材料 | 2023/11/27 | 2024/12/1 | 全国医疗器械生物学评价标准化技术委员会 | 2023年第13号 |
16 | GB/T 16886.23—2023 | 医疗器械生物学评价 第23部分:刺激试验 | 2023/11/27 | 2024/12/1 | 全国医疗器械生物学评价标准化技术委员会 | 2023年第13号 |
17 | GB/T 19042.6—2023 | 医用成像部门的评价及例行试验 第3-6部分:乳腺断层合成成像模式下乳腺摄影X射线设备成像性能验收与 | 2023/11/27 | 2024/12/1 | 全国医用电器标准化技术委员会医用X射线设备及用具分技术委员会 | 2023年第13号 |
18 | GB/T 23101.3—2023 | 外科植入物 羟基磷灰石 第3部分:结晶度和相纯度的化学分析和表征 | 2023/11/27 | 2024/12/1 | 全国外科植入物和矫形器械标准化技术委员会 | 2023年第13号 |
19 | GB/T 23101.4—2023 | 外科植入物 羟基磷灰石 第4部分:涂层粘结强度的测定 | 2023/11/27 | 2024/12/1 | 全国外科植入物和矫形器械标准化技术委员会 | 2023年第13号 |
20 | GB/T 43277.1—2023 | 医用输液(输血)器具用止流夹和流量调节器 第1部分:非液体接触式止流夹和流量调节器 | 2023/11/27 | 2024/12/1 | 全国医用输液器具标准化技术委员会 | 2023年第13号 |
21 | GB/T 43277.2—2023 | 医用输液(输血)器具用止流夹和流量调节器 第2部分:液体接触式刻度流量调节器 | 2023/11/27 | 2024/12/1 | 全国医用输液器具标准化技术委员会 | 2023年第13号 |
22 | GB/T 43278—2023 | 医学实验室 风险管理在医学实验室的应用 | 2023/11/27 | 2024/6/1 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第13号 |
23 | GB/T 43279.1—2023 | 分子体外诊断检验 静脉全血检验前过程的规范 第1部分:分离细胞RNA | 2023/11/27 | 2024/6/1 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第13号 |
24 | GB/T 43279.2—2023 | 分子体外诊断检验 静脉全血检验前过程的规范 第2部分:分离基因组DNA | 2023/11/27 | 2024/6/1 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第13号 |
25 | GB/T 43279.3—2023 | 分子体外诊断检验 静脉全血检验前过程的规范 第3部分:分离血浆循环游离DNA | 2023/11/27 | 2024/6/1 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第13号 |
26 | GB/Z 43280—2023 | 医学实验室 测量不确定度评定指南 | 2023/11/27 | 2024/6/1 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第13号 |
27 | GB/Z 43281—2023 | 即时检验(POCT)设备监督员和操作员指南 | 2023/11/27 | 2024/6/1 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第13号 |
28 | GB/T 24627—2023 | 外科植入物用镍-钛形状记忆合金加工材 | 2023/12/28 | 2025/1/1 | 全国外科植入物和矫形器械标准化技术委员会 | 2023年第20号 |
2023年发布的医疗器械行业标准清单
序号 | 标准编号 | 标准名称 | 发布日期 | 实施日期 | 归口单位 | 发布公告 |
1 | YY 0054—2023 | 血液透析设备 | 2023/1/13 | 2026/1/15 | 全国医用体外循环设备标准化技术委员会 | 2023年第8号 |
2 | YY/T 0506.1—2023 | 医用手术单、手术衣和洁净服 第1部分:通用要求 | 2023/1/13 | 2024/1/15 | 山东省医疗器械和药品包装检验研究院 | 2023年第8号 |
3 | YY/T 0606.15—2023 | 组织工程医疗产品 评价基质及支架免疫反应的试验方法:淋巴细胞增殖试验 | 2023/1/13 | 2024/1/15 | 全国外科植入物和矫形器械标准化技术委员会组织工程医疗器械产品分技术委员会 | 2023年第8号 |
4 | YY/T 0720—2023 | 一次性使用产包 通用要求 | 2023/1/13 | 2024/1/15 | 全国计划生育器械标准化技术委员会 | 2023年第8号 |
5 | YY/T 0730—2023 | 心血管外科植入物和人工器官 心肺旁路和体外膜肺氧合(ECMO)使用的一次性使用管道套包的要求 | 2023/1/13 | 2024/1/15 | 全国医用体外循环设备标准化技术委员会 | 2023年第8号 |
6 | YY 0777—2023 | 射频热疗设备 | 2023/1/13 | 2026/1/15 | 全国医用电器标准化技术委员会物理治疗设备分技术委员会 | 2023年第8号 |
7 | YY/T 0870.7—2023 | 医疗器械遗传毒性试验 第7部分:哺乳动物体内碱性 | 2023/1/13 | 2024/1/15 | 全国医疗器械生物学评价标准化技术委员会 | 2023年第8号 |
8 | YY/T 1106—2023 | 电动手术台 | 2023/1/13 | 2026/1/15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第8号 |
9 | YY/T 1199—2023 | 甘油三酯测定试剂盒(酶法) | 2023/1/13 | 2023/7/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第8号 |
10 | YY/T 1240—2023 | D-二聚体测定试剂盒 | 2023/1/13 | 2023/7/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第8号 |
11 | YY/T 1473—2023 | 医疗器械标准化工作指南 涉及安全内容的标准制定 | 2023/1/13 | 2024/1/15 | 全国医疗器械质量管理和通用要求标准化技术委员会 | 2023年第8号 |
12 | YY/T 1719—2023 | 正电子发射断层成像及磁共振成像设备通用技术要求 | 2023/1/13 | 2026/1/15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第8号 |
13 | YY/T 1789.6—2023 | 体外诊断检验系统 性能评价方法 第6部分:定性试剂的精密度、诊断灵敏度和 | 2023/1/13 | 2024/1/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第8号 |
14 | YY/T 1840—2023 | 医用磁共振成像设备通用 | 2023/1/13 | 2026/1/15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第8号 |
15 | YY/T 1842.7—2023 | 医疗器械 医用贮液容器输送系统用连接件 第7部分:血管内输液用连接件 | 2023/1/13 | 2024/1/15 | 全国医用输液器具标准化技术委员会 | 2023年第8号 |
16 | YY/T 1850—2023 | 男用避孕套 聚氨酯避孕套的技术要求与试验方法 | 2023/1/13 | 2024/1/15 | 全国计划生育器械标准化技术委员会 | 2023年第8号 |
17 | YY/T 1861—2023 | 医学影像存储与传输系统软件专用技术条件 | 2023/1/13 | 2024/1/15 | 全国医用电器标准化技术委员会医用X射线设备及用具分技术委员会 | 2023年第8号 |
18 | YY/T 1862—2023 | 冠状动脉CT影像处理软件专用技术条件 | 2023/1/13 | 2024/1/15 | 全国医用电器标准化技术委员会医用X射线设备及用具分技术委员会 | 2023年第8号 |
19 | YY/T 1863—2023 | 纳米医疗器械生物学评价 含纳米银敷料中纳米银颗粒和银离子的释放与表征方法 | 2023/1/13 | 2024/1/15 | 全国医疗器械生物学评价标准化技术委员会纳米医疗器械生物学评价分技术委员会 | 2023年第8号 |
20 | YY/T 1867—2023 | 运动医学植入器械 带线锚钉 | 2023/1/13 | 2024/1/15 | 全国外科植入物和矫形器械标准化技术委员会 | 2023年第8号 |
21 | YY/T 1868—2023 | 乙型肝炎病毒核心抗体检测试剂盒(发光免疫分析法) | 2023/1/13 | 2024/1/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第8号 |
22 | YY/T 1869—2023 | 探测器阵列剂量测量系统 性能和试验方法 | 2023/1/13 | 2024/7/15 | 全国医用电器标准化技术委员会放射治疗、核医学和放射剂量学设备分技术委员会 | 2023年第8号 |
23 | YY/T 1870—2023 | 液相色谱-质谱法测定试剂盒通用要求 | 2023/1/13 | 2024/1/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第8号 |
24 | YY/T 1871—2023 | 医用隔离衣 | 2023/1/13 | 2024/1/15 | 山东省医疗器械和药品包装检验研究院 | 2023年第8号 |
25 | YY/T 1876—2023 | 组织工程医疗产品 动物源性生物材料DNA残留量 | 2023/1/13 | 2024/1/15 | 全国外科植入物和矫形器械标准化技术委员会组织工程医疗器械产品分技术委员会 | 2023年第8号 |
26 | YY/T 1878—2023 | 正电子发射断层成像装置数字化技术要求 | 2023/1/13 | 2024/7/15 | 全国医用电器标准化技术委员会放射治疗、核医学和放射剂量学设备分技术委员会 | 2023年第8号 |
27 | YY/T 1886—2023 | 牙科学 胶囊装银汞合金 | 2023/1/13 | 2024/1/15 | 全国口腔材料和器械设备标准化技术委员会 | 2023年第8号 |
28 | YY 9706.230—2023 | 医用电气设备 第2-30部分:自动无创血压计的基本安全和基本性能专用要求 | 2023/1/13 | 2026/1/15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第8号 |
29 | YY 9706.246—2023 | 医用电气设备 第2-46部分:手术台的基本安全和基本性能专用要求 | 2023/1/13 | 2026/1/15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第8号 |
30 | YY 9706.249—2023 | 医用电气设备 第2-49部分:多参数患者监护仪的基本安全和基本性能专用要求 | 2023/1/13 | 2026/1/15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第8号 |
31 | YY 9706.261—2023 | 医用电气设备 第2-61部分:脉搏血氧设备的基本安全和基本性能专用要求 | 2023/1/13 | 2026/1/15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第8号 |
32 | YY 9706.277—2023 | 医用电气设备 第2-77部分:采用机器人技术的辅助手术设备的基本安全和基本性能专用要求 | 2023/1/13 | 2026/1/15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第8号 |
33 | YY/T 1888—2023 | 重组人源化胶原蛋白 | 2023/1/18 | 2023/7/20 | 国家药监局医疗器械技术审评中心 | 2023年第14号 |
34 | YY/T 0128—2023 | 医用诊断X射线辐射防护器具 装置及用具 | 2023/3/14 | 2024/5/1 | 全国医用电器标准化技术委员会医用X射线设备及用具分技术委员会 | 2023年第29号 |
35 | YY 0499—2023 | 麻醉和呼吸设备 气管插管用喉镜 | 2023/3/14 | 2026/5/1 | 全国麻醉和呼吸设备标准化技术委员会 | 2023年第29号 |
36 | YY/T 0688.1—2023 | 感染病原体敏感性试验与抗微生物药物敏感性试验设备的性能评价 第1部分:抗微生物药物对感染性疾病相关的快速生长需氧菌的体外活性检测的肉汤微量稀释参考方法 | 2023/3/14 | 2023/11/1 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第29号 |
37 | YY 0970—2023 | 医疗保健产品灭菌 一次性使用动物源性医疗器械的液体化学灭菌剂 医疗器械灭菌过程的特征、开发、确认和常规控制的要求 | 2023/3/14 | 2026/5/1 | 全国消毒技术与设备标准化技术委员会 | 2023年第29号 |
38 | YY/T 1268—2023 | 环氧乙烷灭菌的产品追加和过程等效 | 2023/3/14 | 2024/5/1 | 全国消毒技术与设备标准化技术委员会 | 2023年第29号 |
39 | YY/T 1411—2023 | 牙科学 牙科治疗机水路生物膜处理的试验方法 | 2023/3/14 | 2024/5/1 | 全国口腔材料和器械设备标准化技术委员会齿科设备与器械分技术 | 2023年第29号 |
40 | YY/T 1789.5—2023 | 体外诊断检验系统 性能评价方法 第5部分:分析 | 2023/3/14 | 2024/5/1 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第29号 |
41 | YY/T 1856—2023 | 血液、静脉药液、灌洗液加温器安全通用要求 | 2023/3/14 | 2025/5/1 | 全国医用输液器具标准化技术委员会 | 2023年第29号 |
42 | YY/T 1866—2023 | 一次性使用无菌肛肠套扎器 胶圈或弹力线式 | 2023/3/14 | 2024/5/1 | 全国外科器械标准化 | 2023年第29号 |
43 | YY/T 1874—2023 | 有源植入式医疗器械 电磁兼容 植入式心脏起搏器、植入式心律转复除颤器和心脏再同步器械的电磁兼容测试细则 | 2023/3/14 | 2024/5/1 | 全国外科植入物和矫形器械标准化技术委员会有源植入物分技术 | 2023年第29号 |
44 | YY/T 1882—2023 | 梅毒螺旋体抗体检测试剂盒(发光免疫分析法) | 2023/3/14 | 2024/11/1 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第29号 |
45 | YY/T 1883—2023 | Rh血型C、c、E、e抗原检测卡(柱凝集法) | 2023/3/14 | 2024/5/1 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第29号 |
46 | YY 9706.231—2023 | 医用电气设备 第2-31部分:带内部电源的体外心脏起搏器的基本安全和基本性能专用要求 | 2023/3/14 | 2026/5/1 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第29号 |
47 | YY 9706.256—2023 | 医用电气设备 第2-56部分:用于体温测量的临床体温计的基本安全和基本性能专用要求 | 2023/3/14 | 2026/5/1 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第29号 |
48 | YY 9706.278—2023 | 医用电气设备 第2-78部分:康复、评定、代偿或缓解用医用机器人的基本安全和基本性能专用要求 | 2023/3/14 | 2026/5/1 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第29号 |
49 | YY 9706.279—2023 | 医用电气设备 第2-79部分:用于呼吸功能障碍的呼吸支持设备的基本安全和基本性能专用要求 | 2023/3/14 | 2026/5/1 | 全国麻醉和呼吸设备 | 2023年第29号 |
50 | YY 9706.280—2023 | 医用电气设备 第2-80部分:用于呼吸功能不全的呼吸支持设备的基本安全和基本性能专用要求 | 2023/3/14 | 2026/5/1 | 全国麻醉和呼吸设备 | 2023年第29号 |
51 | YY 9706.284—2023 | 医用电气设备 第2-84部分:紧急医疗服务环境用呼吸机的基本安全和基本性能专用要求 | 2023/3/14 | 2026/5/1 | 全国麻醉和呼吸设备 | 2023年第29号 |
52 | YY/T 0862—2023 | 眼科光学 眼内填充物 | 2023/3/14 | 2024/5/1 | 全国医用光学和仪器 | 2023年第29号 |
53 | YY/T 0893—2023 | 医用气体混合器 独立气体混合器 | 2023/3/14 | 2024/5/1 | 全国麻醉和呼吸设备 | 2023年第29号 |
54 | YY 0272—2023 | 牙科学 氧化锌/丁香酚水门汀和不含丁香酚的氧化锌水门汀 | 2023/6/20 | 2025/7/1 | 全国口腔材料和器械设备标准化技术委员会 | 2023年第82号 |
55 | YY/T 0338—2023 | 气管切开插管和接头 | 2023/6/20 | 2024/7/1 | 山东省医疗器械和药品包装检验研究院 | 2023年第82号 |
56 | YY 0503—2023 | 环氧乙烷灭菌器 | 2023/6/20 | 2025/7/1 | 全国消毒技术与设备 | 2023年第82号 |
57 | YY/T 0776—2023 | 肝脏射频消融治疗设备 | 2023/6/20 | 2025/7/1 | 全国医用电器标准化技术委员会物理治疗设备分技术委员会 | 2023年第82号 |
58 | YY 0793.3—2023 | 血液透析和相关治疗用液体的制备和质量管理 第3部分:血液透析和相关治疗用浓缩物 | 2023/6/20 | 2025/7/1 | 全国医用体外循环设备标准化技术委员会 | 2023年第82号 |
59 | YY/T 0907—2023 | 医用无针注射器 要求及 | 2023/6/20 | 2024/7/1 | 全国医用注射器(针) | 2023年第82号 |
60 | YY 0989.3—2023 | 手术植入物 有源植入式医疗器械 第3部分:植入式 | 2023/6/20 | 2026/7/1 | 全国外科植入物和矫形器械标准化技术委员会有源植入物分技术 | 2023年第82号 |
61 | YY/T 0992—2023 | 内镜清洗工作站 | 2023/6/20 | 2024/7/1 | 全国消毒技术与设备标准化技术委员会 | 2023年第82号 |
62 | YY/T 1437—2023 | 医疗器械 GB/T 42062应用指南 | 2023/6/20 | 2024/7/1 | 全国医疗器械质量管理和通用要求标准化技术委员会 | 2023年第82号 |
63 | YY/T 1754.3—2023 | 医疗器械临床前动物研究 第3部分:用于评价补片组织学反应与生物力学性能的动物腹壁切口疝模型 | 2023/6/20 | 2024/7/1 | 全国医疗器械生物学评价标准化技术委员会 | 2023年第82号 |
64 | YY/T 1766.3—2023 | X射线计算机体层摄影设备图像质量评价方法 第3部分:双能量成像与能谱应用性能评价 | 2023/6/20 | 2025/1/1 | 全国医用电器标准化技术委员会医用X射线设备及用具分技术委员会 | 2023年第82号 |
65 | YY/T 1873—2023 | 麻醉和呼吸设备 笑气吸入镇静镇痛装置 | 2023/6/20 | 2024/7/1 | 全国麻醉和呼吸设备 | 2023年第82号 |
66 | YY 1881—2023 | 医用正压送风式呼吸器 | 2023/6/20 | 2025/7/1 | 医用生物防护产品标准化技术归口单位 | 2023年第82号 |
67 | YY/T 1884—2023 | 固定式含铜宫内节育器 | 2023/6/20 | 2024/7/1 | 全国计划生育器械标准化技术委员会 | 2023年第82号 |
68 | YY 1885—2023 | 传染病患者运送负压隔离舱 | 2023/6/20 | 2025/7/1 | 医用生物防护产品标准化技术归口单位 | 2023年第82号 |
69 | YY 1887—2023 | 医用正压防护服 | 2023/6/20 | 2025/7/1 | 医用生物防护产品标准化技术归口单位 | 2023年第82号 |
70 | YY/T 1894—2023 | 医用磁共振设备可靠性指标验证方法 | 2023/6/20 | 2024/7/1 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第82号 |
71 | YY/T 1896—2023 | 光谱辐射治疗设备波长范围界定方法 | 2023/6/20 | 2024/7/1 | 全国医用电器标准化技术委员会物理治疗设备分技术委员会 | 2023年第82号 |
72 | YY/T 1897—2023 | 纳米医疗器械生物学评价 遗传毒性试验 体外哺乳动物细胞微核试验 | 2023/6/20 | 2024/7/1 | 全国医疗器械生物学评价标准化技术委员会纳米医疗器械生物学评价分技术委员会 | 2023年第82号 |
73 | YY/T 1899—2023 | 可吸收医疗器械植入后组织病理学样本制备与评价方法 | 2023/6/20 | 2024/7/1 | 全国医疗器械生物学评价标准化技术委员会 | 2023年第82号 |
74 | YY/T 0290.5—2023 | 眼科光学 人工晶状体 第5部分:生物相容性 | 2023/9/5 | 2024/9/15 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术委员会 | 2023年第118号 |
75 | YY 0304—2023 | 等离子喷涂羟基磷灰石涂层 钛基牙种植体 | 2023/9/5 | 2026/9/15 | 全国口腔材料和器械设备标准化技术委员会 | 2023年第118号 |
76 | YY 0306—2023 | 热辐射类治疗设备通用技术要求 | 2023/9/5 | 2026/9/15 | 全国医用电器标准化技术委员会物理治疗设备分技术委员会 | 2023年第118号 |
77 | YY 0451—2023 | 一次性使用便携式输注泵 非电驱动 | 2023/9/5 | 2026/9/15 | 全国医用输液器具标准化技术委员会 | 2023年第118号 |
78 | YY/T 0466.1—2023 | 医疗器械 用于制造商提供信息的符号 第1部分:通用要求 | 2023/9/5 | 2025/9/15 | 全国医疗器械质量管理和通用要求标准化技术委员会 | 2023年第118号 |
79 | YY/T 0675—2023 | 眼科仪器 同视机 | 2023/9/5 | 2024/9/15 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术委员会 | 2023年第118号 |
80 | YY/T 0698.5—2023 | 最终灭菌医疗器械包装材料 第5部分:透气材料与塑料膜组成的可密封组合袋和卷材 要求和试验方法 | 2023/9/5 | 2024/9/15 | 全国医用输液器具标准化技术委员会 | 2023年第118号 |
81 | YY 0717—2023 | 牙科学 根管封闭材料 | 2023/9/5 | 2026/9/15 | 全国口腔材料和器械设备标准化技术委员会 | 2023年第118号 |
82 | YY/T 0767—2023 | 彩色超声影像设备通用技术要求 | 2023/9/5 | 2024/9/15 | 全国医用电器标准化技术委员会医用超声设备分技术委员会 | 2023年第118号 |
83 | YY/T 0773—2023 | 眼科B型超声诊断仪通用技术条件 | 2023/9/5 | 2024/9/15 | 全国医用电器标准化技术委员会医用超声设备分技术委员会 | 2023年第118号 |
84 | YY/T 0841—2023 | 医用电气设备 医用电气设备周期性测试和修理后测试 | 2023/9/5 | 2025/9/15 | 全国医用电器标准化技术委员会 | 2023年第118号 |
85 | YY/T 0851—2023 | 医用防血栓袜 | 2023/9/5 | 2024/9/15 | 山东省医疗器械和药品包装检验研究院 | 2023年第118号 |
86 | YY 0875—2023 | 外科器械 直线型吻合器及组件 | 2023/9/5 | 2026/9/15 | 全国外科器械标准化 | 2023年第118号 |
87 | YY/T 0905—2023 | 牙科学 中央压缩空气源 | 2023/9/5 | 2025/3/15 | 全国口腔材料和器械设备标准化技术委员会齿科设备与器械分技术 | 2023年第118号 |
88 | YY/T 0977—2023 | 麻醉和呼吸设备 口咽通 | 2023/9/5 | 2024/9/15 | 全国麻醉和呼吸设备 | 2023年第118号 |
89 | YY/T 1021.2—2023 | 牙科学 拔牙钳 第2部分:标示 | 2023/9/5 | 2024/9/15 | 全国口腔材料和器械设备标准化技术委员会齿科设备与器械分技术 | 2023年第118号 |
90 | YY/T 1021.3—2023 | 牙科学 拔牙钳 第3部分:设计 | 2023/9/5 | 2024/9/15 | 全国口腔材料和器械设备标准化技术委员会齿科设备与器械分技术 | 2023年第118号 |
91 | YY/T 1028—2023 | 医用内窥镜 纤维内窥镜 | 2023/9/5 | 2024/9/15 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术委员会 | 2023年第118号 |
92 | YY 1277—2023 | 压力蒸汽灭菌器 生物安全性能要求 | 2023/9/5 | 2026/9/15 | 全国消毒技术与设备 | 2023年第118号 |
93 | YY/T 1622.2—2023 | 牙科学 牙周探针 第2部分:标示 | 2023/9/5 | 2024/9/15 | 全国口腔材料和器械设备标准化技术委员会齿科设备与器械分技术 | 2023年第118号 |
94 | YY/T 1833.4—2023 | 人工智能医疗器械 质量要求和评价 第4部分:可追溯性 | 2023/9/5 | 2024/9/15 | 人工智能医疗器械标准化技术归口单位 | 2023年第118号 |
95 | YY/T 1889—2023 | 眼科光学 接触镜护理产品 镜片盒内接触镜护理产品及接触镜的细菌和真菌挑战评估方法 | 2023/9/5 | 2024/9/15 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术委员会 | 2023年第118号 |
96 | YY/T 1890—2023 | 乙型肝炎病毒表面抗原检测试剂盒(免疫层析法) | 2023/9/5 | 2024/9/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第118号 |
97 | YY/T 1893—2023 | Y染色体微缺失检测试剂盒 | 2023/9/5 | 2024/9/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第118号 |
98 | YY/T 1895—2023 | 血管内光学相干断层扫描成像设备 | 2023/9/5 | 2024/9/15 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术委员会 | 2023年第118号 |
99 | YY/T 1900—2023 | 牙科学 牙科银汞合金的耐腐蚀性 | 2023/9/5 | 2024/9/15 | 全国口腔材料和器械设备标准化技术委员会 | 2023年第118号 |
100 | YY/T 1901—2023 | 采用机器人技术的骨科手术导航设备要求及试验方法 | 2023/9/5 | 2024/9/15 | 医用机器人标准化技术归口单位 | 2023年第118号 |
101 | YY/T 1905—2023 | 轻离子束放射治疗计划剂量计算准确性要求 | 2023/9/5 | 2024/9/15 | 全国医用电器标准化技术委员会放射治疗核医学和放射剂量学设备分技术委员会 | 2023年第118号 |
102 | YY/T 1906—2023 | 一次性使用无菌闭合夹 | 2023/9/5 | 2024/9/15 | 全国外科器械标准化技术委员会 | 2023年第118号 |
103 | YY/T 1907—2023 | 人工智能医疗器械 冠状动脉CT影像处理软件 算法性能测试方法 | 2023/9/5 | 2024/9/15 | 人工智能医疗器械标准化技术归口单位 | 2023年第118号 |
104 | YY/T 1908—2023 | 核酸提取仪 | 2023/9/5 | 2024/9/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第118号 |
105 | YY/T 1909—2023 | 医用增材制造 金属粉末床电子束熔融工艺控制和确认要求 | 2023/9/5 | 2024/9/15 | 医用增材制造技术医疗器械标准化技术归口单位 | 2023年第118号 |
106 | YY/T 1910—2023 | 用于增材制造的医用β-磷酸三钙粉末 | 2023/9/5 | 2024/9/15 | 医用增材制造技术医疗器械标准化技术归口单位 | 2023年第118号 |
107 | YY/T 1911—2023 | 医疗器械凝血试验方法 | 2023/9/5 | 2024/9/15 | 全国医疗器械生物学评价标准化技术委员会 | 2023年第118号 |
108 | YY/T 1912—2023 | 用于软组织再生医疗器械的生物学评价与试验 | 2023/9/5 | 2024/9/15 | 全国医疗器械生物学评价标准化技术委员会 | 2023年第118号 |
109 | YY/T 1913—2023 | 医用聚碳酸酯材料中2,2-二(4-羟基苯基)丙烷(双酚A)残留量测定方法 | 2023/9/5 | 2024/9/15 | 全国医疗器械生物学评价标准化技术委员会 | 2023年第118号 |
110 | YY/T 1914—2023 | 人类辅助生殖技术用医疗器械 器具类产品通用要求 | 2023/9/5 | 2024/9/15 | 人类辅助生殖技术用医疗器械标准化技术归口单位 | 2023年第118号 |
111 | YY/T 1915—2023 | 免疫层析试剂盒实验室检测通则 | 2023/9/5 | 2024/3/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第118号 |
112 | YY/T 1916—2023 | 白介素6(IL-6)测定试剂盒(标记免疫分析法) | 2023/9/5 | 2024/9/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第118号 |
113 | YY/T 1917—2023 | 抗Xa测定试剂盒 | 2023/9/5 | 2024/9/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第118号 |
114 | YY/T 1918—2023 | 数字聚合酶链反应分析系统 | 2023/9/5 | 2024/9/15 | 全国医用临床检验实验室和体外诊断系统标准化技术委员会 | 2023年第118号 |
115 | YY/T 1919—2023 | 超声造影成像性能试验方法 | 2023/9/5 | 2024/9/15 | 全国医用电器标准化技术委员会医用超声设备分技术委员会 | 2023年第118号 |
116 | YY/T 1920—2023 | 透析器血液相容性试验 | 2023/9/5 | 2024/9/15 | 全国医用体外循环设备标准化技术委员会 | 2023年第118号 |
117 | YY/T 1921—2023 | 闭环式含铜宫内节育器 | 2023/9/5 | 2024/9/15 | 全国计划生育器械标准化技术委员会 | 2023年第118号 |
118 | YY 0852—2023 | 一次性使用无菌手术膜 | 2023/9/5 | 2026/9/15 | 山东省医疗器械和药品包装检验研究院 | 2023年第118号 |
119 | YY/T 0127.4—2023 | 口腔医疗器械生物学评价 第4部分:骨植入试验 | 2023/11/22 | 2024/12/1 | 全国口腔材料和器械设备标准化技术委员会 | 2023年第149号 |
120 | YY/T 0127.19—2023 | 口腔医疗器械生物学评价 第19部分:亚急性和亚慢性全身毒性试验:植入途径 | 2023/11/22 | 2024/12/1 | 全国口腔材料和器械设备标准化技术委员会 | 2023年第149号 |
121 | YY 0315—2023 | 钛及钛合金牙种植体 | 2023/11/22 | 2026/12/1 | 全国口腔材料和器械设备标准化技术委员会 | 2023年第149号 |
122 | YY 0469—2023 | 医用外科口罩 | 2023/11/22 | 2026/12/1 | 全国医用防护器械 | 2023年第149号 |
123 | YY 0793.2—2023 | 血液透析和相关治疗用液体的制备和质量管理 第2部分:血液透析和相关治疗用水 | 2023/11/22 | 2026/12/1 | 全国医用体外循环设备标准化技术委员会 | 2023年第149号 |
124 | YY/T 0929.3—2023 | 输液用药液过滤器 第3部分:标称孔径0.22μm药液过滤器液体细菌截留试验方法 | 2023/11/22 | 2024/12/1 | 全国医用输液器具 | 2023年第149号 |
125 | YY/T 0969—2023 | 一次性使用医用口罩 | 2023/11/22 | 2025/12/1 | 全国医用防护器械 | 2023年第149号 |
126 | YY 1042—2023 | 牙科学 聚合物基修复材料 | 2023/11/22 | 2026/12/1 | 全国口腔材料和器械设备标准化技术委员会 | 2023年第149号 |
127 | YY/T 1842.3—2023 | 医疗器械 医用贮液容器输送系统用连接件 第3部分:胃肠道应用 | 2023/11/22 | 2024/12/1 | 全国医用输液器具 | 2023年第149号 |
128 | YY/T 1904—2023 | 医用防护眼(面)罩 | 2023/11/22 | 2025/12/1 | 全国医用防护器械 | 2023年第149号 |
129 | YY/T 1928—2023 | 预期用于磁共振环境的医用电气设备的术语和分类 | 2023/11/22 | 2024/12/1 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第149号 |
130 | YY/T 0003—2023 | 手动病床 | 2023/11/22 | 2025/12/1 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | 2023年第149号 |
131 | YY/T 0489—2023 | 一次性使用无菌引流导管及辅助器械 | 2023/11/22 | 2024/12/1 | 全国医用输液器具 | 2023年第149号 |
2023年发布的医疗器械行业标准修改单清单
序号 | 标准编号 | 标准名称 | 发布日期 | 实施日期 | 归口单位 | 发布公告 |
1 | YY 0068.4—2009 | 医用内窥镜 硬性内窥镜 | 2009/12/30 | 2011/6/1 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术委员会 | 2023年第107号 |
2 | YY/T 0322—2018 | 高频电灼治疗仪 | 2018/9/28 | 2020/4/1 | 全国医用电器标准化技术委员会物理治疗设备分技术委员会 | 2023年第107号 |
3 | YY 0649—2016 | 电位治疗设备 | 2016/7/29 | 2018/6/1 | 全国医用电器标准化技术委员会物理治疗设备分技术委员会 | 2023年第107号 |
4 | YY/T 0718—2009 | 眼科仪器 检影镜 | 2009/6/16 | 2010/12/1 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术委员会 | 2023年第107号 |
5 | YY/T 0719.4—2009 | 眼科光学 接触镜护理产品 第4部分:抗微生物防腐有效性试验及测定抛弃日期 | 2009/6/16 | 2010/12/1 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术委员会 | 2023年第107号 |
6 | YY/T 0763—2009 | 医用内窥镜 照明用光缆 | 2009/12/30 | 2011/6/1 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术委员会 | 2023年第107号 |
7 | YY/T 0994—2015 | 磁刺激设备 | 2015/3/2 | 2016/1/1 | 全国医用电器标准化技术委员会物理治疗设备分技术委员会 | 2023年第107号 |
8 | YY/T 0919—2014 | 无源外科植入物 关节置换植入物 膝关节置换植入物的专用要求 | 2014/6/17 | 2015/7/1 | 全国外科植入物和矫形器械标准化技术委员会骨科植入物分技术 | 2023年第149号 |
9 | YY/T 0951—2015 | 干扰电治疗设备 | 2015/3/2 | 2017/1/1 | 全国医用电器标准化技术委员会物理治疗设备分技术委员会 | 2023年第149号 |
10 | YY/T 0966—2014 | 外科植入物 金属材料 纯钽 | 2014/6/17 | 2015/7/1 | 全国外科植入物和矫形器械标准化技术委员会骨科植入物分技术 | 2023年第149号 |
11 | YY/T 1426.1—2016 | 外科植入物 全膝关节假体的磨损 第1部分:载荷控制的磨损试验机的载荷和位移参数及相关的试验环境条件 | 2016/1/26 | 2017/1/1 | 全国外科植入物和矫形器械标准化技术委员会骨科植入物分技术 | 2023年第149号 |
12 | YY/T 1426.2—2016 | 外科植入物 全膝关节假体的磨损 第2部分:测量方法 | 2016/1/26 | 2017/1/1 | 全国外科植入物和矫形器械标准化技术委员会骨科植入物分技术 | 2023年第149号 |
13 | YY/T 1426.3—2017 | 外科植入物 全膝关节假体的磨损 第3部分:位移控制的磨损试验机的载荷和位移参数及相关的试验环境条件 | 2017/9/25 | 2018/10/1 | 全国外科植入物和矫形器械标准化技术委员会骨科植入物分技术 | 2023年第149号 |
14 | YY/T 1447—2016 | 外科植入物 植入材料磷灰石形成能力的体外评估 | 2016/1/26 | 2017/1/1 | 全国外科植入物和矫形器械标准化技术委员会骨科植入物分技术 | 2023年第149号 |
新版医用电气设备标准清单
序号 | 标准编号 | 标准名称 | 代替标准号 | 采标号 | 发布日期 | 实施日期 | 归口单位 |
1 | GB 9706.1—2020 | 医用电气设备 第1部分: | GB 9706.1—2007 GB 9706.15—2008 | IEC 60601-1:2012 | 2020-04-09 | 2023-05-01 | 国家药品监督 |
2 | GB 9706.103—2020 | 医用电气设备 第1-3部分:基本安全和基本性能的通用要求 并列标准:诊断X射线设备的辐射防护 | GB 9706.12—1997 | IEC 60601-1-3:2013 | 2020-12-24 | 2023-05-01 | 国家药品监督 |
3 | GB 9706.201—2020 | 医用电气设备 第2-1部分:能量为1MeV至50MeV电子加速器基本安全和基本性能专用要求 | GB 9706.5—2008 | IEC 60601-2-1:2014 | 2020-12-24 | 2023-05-01 | 国家药品监督 |
4 | GB 9706.202—2021 | 医用电气设备 第2-2部分:高频手术设备及高频附件的基本安全和基本性能专用 | GB 9706.4—2009 | IEC 60601-2-2:2017 | 2021-12-01 | 2023-05-01 | 国家药品监督 |
5 | GB 9706.203—2020 | 医用电气设备 第2-3部分:短波治疗设备的基本安全和基本性能专用要求 | IEC 60601-2-3:2016 | 2020-05-29 | 2023-05-01 | 国家药品监督 | |
6 | GB 9706.204—2022 | 医用电气设备 第2-4部分:心脏除颤器的基本安全和基本性能专用要求 | GB 9706.8—2009 | IEC 60601-2-4:2018 | 2022-07-13 | 2024-08-01 | 国家药品监督 |
7 | GB 9706.205—2020 | 医用电气设备 第2-5部分:超声理疗设备的基本安全和基本性能专用要求 | GB 9706.7—2008 | IEC 60601-2-5:2009 | 2020-07-23 | 2023-05-01 | 国家药品监督 |
8 | GB 9706.206—2020 | 医用电气设备 第2-6部分:微波治疗设备的基本安全和基本性能专用要求 | GB 9706.6—2007 | IEC 60601-2-6:2016 | 2020-07-23 | 2023-05-01 | 国家药品监督 |
9 | GB 9706.208—2021 | 医用电气设备 第2-8部分:能量为10kV至1MV 治疗X射线设备的基本安全和基本性能专用要求 | GB 9706.10—1997 | IEC 60601-2-8:2015 | 2021-08-10 | 2023-05-01 | 国家药品监督 |
10 | GB 9706.211—2020 | 医用电气设备 第2-11部分:γ射束治疗设备的基本安全和基本性能专用要求 | GB 9706.17—2009 | IEC 60601-2-11:2013 | 2020-12-24 | 2023-05-01 | 国家药品监督 |
11 | GB 9706.212—2020 | 医用电气设备 第2-12部分:重症护理呼吸机的基本安全和基本性能专用要求 | GB 9706.28—2006 | ISO 80601-2-12:2011 | 2020-04-09 | 2023-05-01 | 全国麻醉和呼吸设备标准化技术委员会 |
12 | GB 9706.213—2021 | 医用电气设备 第2-13部分:麻醉工作站的基本安全和基本性能专用要求 | GB 9706.29—2006 | ISO 80601-2-13:2011 | 2021-12-01 | 2023-05-01 | 国家药品监督 |
13 | GB 9706.216—2021 | 医用电气设备 第2-16部分:血液透析、血液透析滤过和血液滤过设备的基本安全和基本性能专用要求 | GB 9706.2—2003 | IEC 60601-2-16:2018 | 2021-08-10 | 2023-05-01 | 国家药品监督 |
14 | GB 9706.217—2020 | 医用电气设备 第2-17部分:自动控制式近距离治疗后装设备的基本安全和基本性能专用要求 | GB 9706.13—2008 | IEC 60601-2-17:2013 | 2020-12-24 | 2023-05-01 | 国家药品监督 |
15 | GB 9706.218—2021 | 医用电气设备 第2-18部分:内窥镜设备的基本安全和基本性能专用要求 | GB 9706.19—2000 | IEC 60601-2-18:2009 | 2021-12-01 | 2023-05-01 | 国家药品监督 |
16 | GB 9706.219—2021 | 医用电气设备 第2-19部分:婴儿培养箱的基本安全和基本性能专用要求 | GB 11243—2008 | IEC 60601-2-19:2016 | 2021-10-11 | 2023-05-01 | 国家药品监督 |
17 | GB 9706.222—2022 | 医用电气设备 第2-22部分:外科、整形、治疗和诊断用激光设备的基本安全和基本性能专用要求 | GB 9706.20—2000 | IEC 60601-2-22:2019 | 2022-03-15 | 2024-05-01 | 国家药品监督 |
18 | GB 9706.224—2021 | 医用电气设备 第2-24部分:输液泵和输液控制器的基本安全和基本性能专用要求 | GB 9706.27—2005 | IEC 60601-2-24:2012 | 2021-12-01 | 2023-05-01 | 国家药品监督 |
19 | GB 9706.225—2021 | 医用电气设备 第2-25部分:心电图机的基本安全和基本性能专用要求 | GB 10793—2000 | IEC 60601-2-25:2011 | 2021-12-01 | 2023-05-01 | 国家药品监督 |
20 | GB 9706.226—2021 | 医用电气设备 第2-26部分:脑电图机的基本安全和基本性能专用要求 | GB 9706.26—2005 | IEC 60601-2-26:2012 | 2021-10-11 | 2023-05-01 | 国家药品监督 |
21 | GB 9706.227—2021 | 医用电气设备 第2-27部分:心电监护设备的基本安全和基本性能专用要求 | GB 9706.25—2005 | IEC 60601-2-27:2011 | 2021-10-11 | 2023-05-01 | 国家药品监督 |
22 | GB 9706.228—2020 | 医用电气设备 第2-28部分:医用诊断X射线管组件的基本安全和基本性能专用要求 | GB 9706.11—1997 | IEC 60601-2-28:2017 | 2020-12-24 | 2023-05-01 | 国家药品监督 |
23 | GB 9706.229—2021 | 医用电气设备 第2-29部分:放射治疗模拟机的基本安全和基本性能专用要求 | GB 9706.16—2015 | IEC 60601-2-29:2008 | 2021-08-10 | 2023-05-01 | 国家药品监督 |
24 | GB 9706.236—2021 | 医用电气设备 第2-36部分:体外引发碎石设备的基本安全和基本性能专用要求 | GB 9706.22—2003 | IEC 60601-2-36:2014 | 2021-12-01 | 2023-05-01 | 国家药品监督 |
25 | GB 9706.237—2020 | 医用电气设备 第2-37部分:超声诊断和监护设备的基本安全和基本性能专用要求 | GB 9706.9—2008 | IEC 60601-2-37:2015 | 2020-04-09 | 2023-05-01 | 国家药品监督 |
26 | GB 9706.239—2021 | 医用电气设备 第2-39部分:腹膜透析设备的基本安全和基本性能专用要求 | GB 9706.39—2008 | IEC 60601-2-39:2018 | 2021-08-10 | 2023-05-01 | 国家药品监督 |
27 | GB 9706.243—2021 | 医用电气设备 第2-43部分:介入操作X射线设备的基本安全和基本性能专用要求 | GB 9706.23—2005 | IEC 60601-2-43:2017 | 2021-02-20 | 2023-05-01 | 国家药品监督 |
28 | GB 9706.244—2020 | 医用电气设备 第2-44部分:X射线计算机体层摄影设备的基本安全和基本性能专用要求 | GB 9706.18—2006 | IEC 60601-2-44:2016 | 2020-12-24 | 2023-05-01 | 国家药品监督 |
29 | GB 9706.245—2020 | 医用电气设备 第2-45部分:乳腺X射线摄影设备和乳腺摄影立体定位装置的基本安全和基本性能专用要求 | GB 9706.24—2005 | IEC 60601-2-45:2015 | 2020-12-24 | 2023-05-01 | 国家药品监督 |
30 | GB 9706.254—2020 | 医用电气设备 第2-54部分:X射线摄影和透视设备的基本安全和基本性能专用要求 | IEC 60601-2-54:2018 | 2020-12-24 | 2023-05-01 | 国家药品监督 | |
31 | GB 9706.255—2022 | 医用电气设备 第2-55部分:呼吸气体监护仪的基本安全和基本性能专用要求 | ISO 80601-2-55:2018 | 2022-12-29 | 2026-01-01 | 国家药品监督 | |
32 | GB 9706.260—2020 | 医用电气设备 第2-60部分:牙科设备的基本安全和基本性能专用要求 | IEC 80601-2-60:2012 | 2020-11-17 | 2023-05-01 | 国家药品监督 | |
33 | GB 9706.263—2020 | 医用电气设备 第2-63部分:口外成像牙科X射线机基本安全和基本性能专用要求 | IEC 60601-2-63:2017 | 2020-11-17 | 2023-05-01 | 国家药品监督 | |
34 | GB 9706.265—2021 | 医用电气设备 第2-65部分:口内成像牙科X射线机的基本安全和基本性能专用要求 | IEC 60601-2-65:2017 | 2021-02-20 | 2023-05-01 | 国家药品监督 | |
35 | GB 9706.271—2022 | 医用电气设备 第2-71部分:功能性近红外光谱(NIRS)设备的基本安全和基本性能专用要求 | IEC 80601-2-71:2015 | 2022-12-29 | 2026-01-01 | 国家药品监督 | |
36 | GB 9706.275—2022 | 医用电气设备 第2-75部分:光动力治疗和光动力诊断设备的基本安全和基本性能专用要求 | IEC 60601-2-75:2017 | 2022-12-29 | 2026-01-01 | 国家药品监督 | |
37 | GB 9706.283—2022 | 医用电气设备 第2-83部分:家用光治疗设备的基本安全和基本性能专用要求 | IEC 60601-2-83:2019 | 2022-12-29 | 2026-01-01 | 国家药品监督 | |
38 | GB 9706.290—2022 | 医用电气设备 第2-90部分:高流量呼吸治疗设备的基本安全和基本性能专用要求 | ISO 80601-2-90:2021 | 2022-12-29 | 2026-01-01 | 国家药品监督 | |
39 | YY 9706.102—2021 | 医用电气设备 第1-2部分:基本安全和基本性能的通用要求 并列标准:电磁兼容 要求和试验 | YY 0505—2012 | IEC 60601-1-2:2007 | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会 |
40 | YY/T 9706.106— 2021 | 医用电气设备 第1-6部分:基本安全和基本性能的通用要求 并列标准:可用性 | IEC 60601-1-6:2013 | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会 | |
41 | YY 9706.108—2021 | 医用电气设备 第1-8部分:基本安全和基本性能的通用要求 并列标准:通用要求,医用电气设备和医用电气系统中报警系统的测试和指南 | YY 0709—2009 | IEC 60601-1-8:2006+A1:2012 | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会 |
42 | YY/T 9706.110— 2021 | 医用电气设备 第1-10部分:基本安全和基本性能的通用要求 并列标准:生理闭环控制器开发要求 | IEC 60601-1-10:2007+A1:2013 | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会 | |
43 | YY 9706.111— 2021 | 医用电气设备 第1-11部分:基本安全和基本性能的通用要求 并列标准:在家庭护理环境中使用的医用电气设备和医用电气系统的要求 | IEC 60601-1-11:2015 | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会 | |
44 | YY 9706.112— 2021 | 医用电气设备 第1-12部分:基本安全和基本性能的通用要求 并列标准:预期在紧急医疗服务环境中使用的医用电气设备和医用电气系统的要求 | IEC 60601-1-12:2014 | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会 | |
45 | YY 9706.210—2021 | 医用电气设备 第2-10部分:神经和肌肉刺激器的基本安全和基本性能专用要求 | YY 0607—2007 | IEC 60601-2-10: 2012+AMD1:2016 CSV | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会物理治疗设备分技术委员会 |
46 | YY 9706.220—2021 | 医用电气设备 第2-20部分:婴儿转运培养箱的基本安全和基本性能专用要求 | YY 0827—2011 | IEC 60601-2-20:2009+AMD1:2016 | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
47 | YY 9706.221—2021 | 医用电气设备 第2-21部分:婴儿辐射保暖台的基本安全和基本性能专用要求 | YY 0455—2011 | IEC 60601-2-21:2009/AMD1:2016 | 2021-09-06 | 2024-05-01 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
48 | YY 9706.230—2023 | 医用电气设备 第2-30部分:自动无创血压计的基本安全和基本性能专用要求 | YY 0667—2008 YY 0670—2008 | IEC 80601-2-30:2018 | 2023-01-13 | 2026-01-15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
49 | YY 9706.231—2023 | 医用电气设备 第2-31部分:带内部电源的体外心脏起搏器的基本安全和基本性能专用要求 | YY 0945.2—2015 | IEC 60601-2-31:2020 | 2023-03-14 | 2026-05-01 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
50 | YY 9706.233—2021 | 医用电气设备 第2-33部分:医疗诊断用磁共振设备的基本安全和基本性能专用要求 | YY 0319—2008 | IEC 60601-2-33:2015 | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
51 | YY 9706.234—2021 | 医用电气设备 第2-34部分:有创血压监护设备的基本安全和基本性能专用要求 | YY 0783—2010 | IEC 60601-2-34:2011 | 2021-09-06 | 2024-05-01 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
52 | YY 9706.235—2021 | 医用电气设备 第2-35部分:医用毯、垫或床垫式加热设备的基本安全和基本性能专用要求 | YY 0834—2011 | IEC 80601-2-35:2009+AMD1:2016 CSV | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会物理治疗设备分技术委员会 |
53 | YY 9706.240—2021 | 医用电气设备 第2-40部分:肌电及诱发反应设备的基本安全和基本性能专用要求 | YY 0896—2013 | IEC 60601-2-40:2016 | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
54 | YY 9706.241—2020 | 医用电气设备 第2-41部分:手术无影灯和诊断用照明灯的基本安全和基本性能专用要求 | YY 0627—2008 | IEC 60601-2-41:2013 | 2020-09-27 | 2023-05-01 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术 |
55 | YY 9706.246—2023 | 医用电气设备 第2-46部分:手术台的基本安全和基本性能专用要求 | YY 0570—2013 | IEC 60601-2-46:2016 | 2023-01-13 | 2026-01-15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
56 | YY 9706.247—2021 | 医用电气设备 第2-47部分:动态心电图系统的基本安全和基本性能专用要求 | YY 0885—2013 | IEC 60601-2-47:2012 | 2021-09-06 | 2024-05-01 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
57 | YY 9706.249—2023 | 医用电气设备 第2-49部分:多参数患者监护仪的基本安全和基本性能专用要求 | YY 0668—2008 | IEC 80601-2-49:2018 | 2023-01-13 | 2026-01-15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
58 | YY 9706.250—2021 | 医用电气设备 第2-50部分:婴儿光治疗设备的基本安全和基本性能专用要求 | YY 0669—2008 | IEC 60601-2-50:2009+A1:2016 | 2021-03-09 | 2023-05-01 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术 |
59 | YY 9706.252—2021 | 医用电气设备 第2-52部分:医用病床的基本安全和基本性能专用要求 | YY 0571—2013 | IEC 60601-2-52:2009/AMD1:2015 | 2021-09-06 | 2024-05-01 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
60 | YY 9706.256—2023 | 医用电气设备 第2-56部分:用于体温测量的临床体温计的基本安全和基本性能专用要求 | YY 0785—2010 | ISO 80601-2-56:2017 | 2023-03-14 | 2026-05-01 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
61 | YY 9706.257—2021 | 医用电气设备 第2-57部分:治疗、诊断、监测和整形/医疗美容使用的非激光光源设备基本安全和基本性能的专用要求 | IEC 60601-2-57:2011 | 2021-03-09 | 2023-05-01 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术 | |
62 | YY 9706.258—2022 | 医用电气设备 第2-58部分:眼科手术用晶状体摘除及玻璃体切除设备的基本安全和基本性能专用要求 | IEC 80601-2-58:2016 | 2022-05-18 | 2025-06-01 | 全国光学和光子学标准化技术委员会医用光学和仪器分技术 | |
63 | YY 9706.261—2023 | 医用电气设备 第2-61部分:脉搏血氧设备的基本安全和基本性能专用要求 | YY 0784—2010 | ISO 80601-2-61:2017 | 2023-01-13 | 2026-01-15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 |
64 | YY 9706.262—2021 | 医用电气设备 第2-62部分:高强度超声治疗(HITU)设备的基本安全和基本性能专用要求 | IEC 60601-2-62:2013 | 2021-03-09 | 2023-05-01 | 全国医用电器标准化技术委员会医用超声设备分技术委员会 | |
65 | YY 9706.264—2022 | 医用电气设备 第2-64部分:轻离子束医用电气设备的基本安全和基本性能专用要求 | IEC 60601-2-64:2014 | 2022-05-18 | 2025-06-01 | 全国医用电器标准化技术委员会放射治疗、核医学和放射剂量学设备分技术 | |
66 | YY 9706.268—2022 | 医用电气设备 第2-68部分:电子加速器、轻离子束治疗设备和放射性核素射束治疗设备用的X射线图像引导放射治疗设备的基本安全和基本性能专用要求 | IEC 60601-2-68:2014 | 2022-05-18 | 2025-06-01 | 全国医用电器标准化技术委员会放射治疗、核医学和放射剂量学设备分技术 | |
67 | YY 9706.269—2021 | 医用电气设备 第2-69部分:氧气浓缩器的基本安全和基本性能专用要求 | YY 0732—2009 | ISO 80601-2-69:2014 | 2021-03-09 | 2023-05-01 | 全国麻醉和呼吸设备标准化技术委员会 |
68 | YY 9706.270—2021 | 医用电气设备 第2-70部分:睡眠呼吸暂停治疗设备的基本安全和基本性能专用要求 | YY 0671.1—2009 | ISO 80601-2-70:2015 | 2021-09-06 | 2024-05-01 | 全国麻醉和呼吸设备标准化技术委员会 |
69 | YY 9706.272—2021 | 医用电气设备 第2-72部分:依赖呼吸机患者使用的家用呼吸机的基本安全和基本性能专用要求 | YY 0600.2—2007 | ISO 80601-2-72:2015 | 2021-09-06 | 2024-05-01 | 全国麻醉和呼吸设备标准化技术委员会 |
70 | YY 9706.274—2022 | 医用电气设备 第2-74部分:呼吸湿化设备的基本安全和基本性能专用要求 | YY 0786—2010 | ISO 80601-2-74:2017 | 2022-01-13 | 2025-05-01 | 全国麻醉和呼吸设备标准化技术委员会 |
71 | YY 9706.277—2023 | 医用电气设备 第2-77部分:采用机器人技术的辅助手术设备的基本安全和基本性能专用要求 | IEC 80601-2-77:2019 | 2023-01-13 | 2026-01-15 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | |
72 | YY 9706.278—2023 | 医用电气设备 第2-78部分:康复、评定、代偿或缓解用医用机器人的基本安全和基本性能专用要求 | IEC 80601-2-78:2019 | 2023-03-14 | 2026-05-01 | 全国医用电器标准化技术委员会医用电子仪器分技术委员会 | |
73 | YY 9706.279—2023 | 医用电气设备 第2-79部分:用于呼吸功能障碍的呼吸支持设备的基本安全和基本性能专用要求 | YY 0600.1—2007 | ISO 80601-2-79:2018 | 2023-03-14 | 2026-05-01 | 全国麻醉和呼吸设备标准化技术委员会 |
74 | YY 9706.280—2023 | 医用电气设备 第2-80部分:用于呼吸功能不全的呼吸支持设备的基本安全和基本性能专用要求 | YY 0600.1—2007 | ISO 80601-2-80:2018 | 2023-03-14 | 2026-05-01 | 全国麻醉和呼吸设备标准化技术委员会 |
75 | YY 9706.284—2023 | 医用电气设备 第2-84部分:紧急医疗服务环境用呼吸机的基本安全和基本性能专用要求 | YY 0600.3—2007 | ISO 80601-2-84:2020 | 2023-03-14 | 2026-05-01 | 全国麻醉和呼吸设备标准化技术委员会 |
相关推荐
CIO提供以下相关文库下载、合规服务以及线上培训课程学习。























