海图生物:细胞治疗产品GMP体系搭建与认证服务
CIO协助搭建了完整、可落地、可运行的细胞治疗产品GMP合规体系,使其在10个月内实现从基础薄弱到通过专业审计的跨越式提升,直接支撑了临床研究的推进。该服务有效解决了企业过渡性中试车间的合规难题,在不进行过度硬件改造的前提下,通过精准的差距分析、体系完善与验证落地,让现有场地满足Ⅱ期临床前生产要求,避免了无效投入与资源浪费。
项目背景
2024年底,海图生物科技(上海)有限责任公司(以下简称“海图生物”)在完成早期研发并准备进入中试放大阶段后,正式寻求专业的GMP合规咨询支持。该企业专注于靶向细胞治疗产品研发,核心产品包括靶向树突细胞疫苗等。此前,其仅接触过ISO质量管理体系认证,虽具备基础的体系认知,但相关体系并未真正融入日常运营,且因缺乏持续维护,无法通过后续年度监督审核,GMP合规基础较为薄弱。
海图生物对自身发展阶段与场地定位有着清晰认知。现有中试车间仅用于Ⅱ期临床前研究,不具备满足Ⅲ期临床及商业化生产的规模条件,未来规划新建更大规模的生产场地,故现阶段不进行过度投资。基于务实稳健的发展理念,企业坚持不敷衍、不投机,扎实完成当前阶段的合规工作,确保每一步建设均符合临床研究需求。
此次合作的核心诉求明确:短期需为研究者发起的Ⅱ期临床研究提供合规依据,证明样品系在符合GMP条件下生产;中期要为Ⅱ期临床前试验提供质量可靠、数据完整的样品;长期则希望当前搭建的体系与培养的能力能够平移至未来新场地,实现合规投入的有效延续。

项目过程
项目于2025年3月正式启动,以体系建设、硬件完善、人员赋能与验证先行相结合为整体策略,严格遵循不过度设计、合规不减配、体系可移植三大原则,历时10个月完成了从搭建到通过审计的全流程工作。
一、GMP差距分析
由专家团队对企业车间硬件、文件体系、人员能力及验证状态展开全面评估,输出差距分析报告并明确重点改进事项,为后续工作奠定基础。
二、硬件确认与管理完善
在不进行大规模改造的前提下,完成洁净空调、关键设备的验证工作,并搭建环境监测体系。
三、体系完善与人员赋能
联合企业人员编写了三百余份合规且贴合实操的管理规程、操作规程等文件,同时通过闭环培训提升全员GMP意识,推动实现从被动执行到主动思考的转变。
四、试验
在核心验证阶段,企业顺利完成连续3批无菌模拟试验,同步推进清洁、分析方法、运输等验证工作并完成文件归档,在此基础上开展核心产品连续3批工艺验证,确保生产工艺稳定可靠。
五、模拟审计
正式审计前,企业需开展多轮自查与模拟检查,提前排查问题并完成闭环整改,随后向审计机构提交正式审计申请。
2026年2月,公司接受了为期2天的GMP符合性审计。针对审计过程中提出的缺陷项,在专业辅导下完成了全面整改并提交整改报告,最终顺利通过审计,获得了GMP符合性证书。
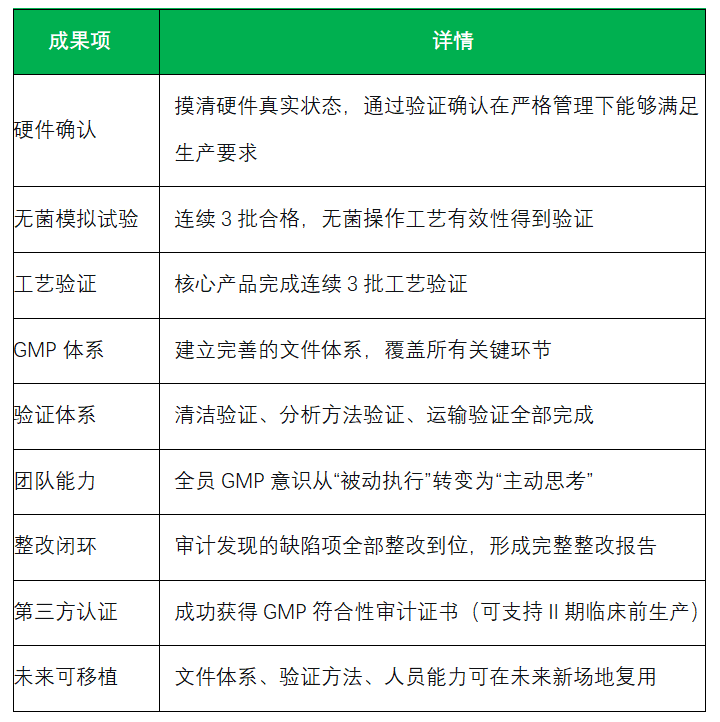
典型意义
CIO合规保证组织协助海图生物搭建了完整、可落地、可运行的细胞治疗产品GMP合规体系,使其在10个月内实现从基础薄弱到通过专业审计的跨越式提升,直接支撑了临床研究的推进。该服务有效解决了企业过渡性中试车间的合规难题,在不进行过度硬件改造的前提下,通过精准的差距分析、体系完善与验证落地,让现有场地满足Ⅱ期临床前生产要求,避免了无效投入与资源浪费。
我们协助企业建立的文件体系、验证方法与人员能力具备高度可移植性,使本次合规投入成为可延续复用的长期资产,而非沉没成本,为企业未来Ⅲ期临床及商业化场地建设奠定了扎实基础。服务全程以数据与实操为核心,推动团队从被动执行转为主动合规,真正将GMP理念融入日常运营,大幅降低了临床样品质量风险,保障了临床试验结果可靠、过程合规。最终帮助企业顺利取得GMP符合性审计证书,满足Ⅱ期临床研究申报与Ⅱ期临床前样品生产的合规要求,为企业后续研发、临床推进与行业合作提供了关键资质与信任背书。












