基本信息
1、办理部门:国家药品监督管理局
2、办理方式:网上办理
3、办理地点:(1)北京市朝阳区建国路128号;(2)北京市西城区宣武门西大街28号大成广场3门一层
4、药监咨询:010-85242306或010-88331793 CIO咨询:400-003-0818
受理条件
申请事项属于本行政机关职权范围,申请材料齐全、符合法定形式,或者申请人按照本行政机关的要求提交全部补正申请材料的,受理行政许可申请。
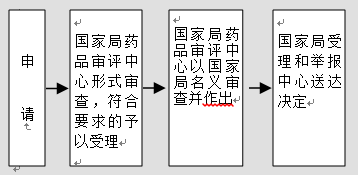
办理流程
流程文字说明
法定办结时限:5个工作日;承诺办结时限:5个工作日
1、受理;
2、审查;
3、行政许可决定;
4、送达。
申请材料
1、港澳台生产医药产品备案表。
2、港、澳、台生产已上市化学药品/生物制品/中药变更申报资料。
常见问题
问题1:药品生产过程中出现变更,需要进行备案吗?
答:《中华人民共和国药品管理法》(2019年)第七十九条:“对药品生产过程中的变更,按照其对药品安全性、有效性和质量可控性的风险和产生影响的程度,实行分类管理。属于重大变更的,应当经国务院药品监督管理部门批准,其他变更应当按照国务院药品监督管理部门的规定备案或者报告。”
本办事指南摘自药监局官网,如有变动,以官方发布为准。