基本信息
1、办理部门:江苏省药品监督管理局
2、办理方式:网上办理
3、办理地点:南京市建邺区汉中门大街145号江苏省政务服务中心省药监局窗口
4、咨询电话: 12315 CIO咨询:400-003-0818
受理条件
《中华人民共和国行政许可法》第三十二条第五项: 申请事项属于本行政机关职权范围,申请材料齐全、符合法定形式,或者申请人按照本行政机关的要求提交全部补正申请材料的,应当受理行政许可申请。
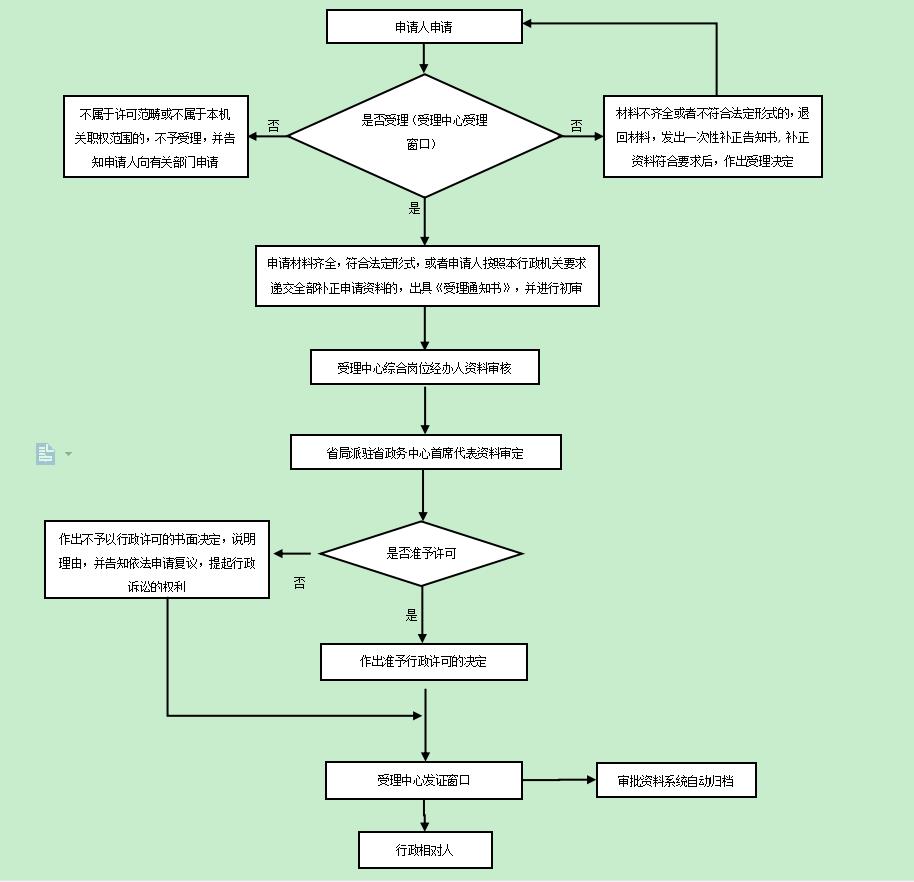
办理流程
流程文字说明
1、受理(时限:1个工作日)
办理结果:申请材料存在可以当场更正的错误的,应当允许有权更正人当场予以更正,由更正人在更正处签名或者盖章、注明更正日期;经确认申请材料齐全,符合法定形式的,应当决定予以受理。申请材料不齐全或者不符合法定形式的,应当当场告知申请人需要补正的全部内容。
2、审查(时限:8个工作日)
办理结果:根据《医疗器械注册管理办法》,对申请材料进行实质内容审查,并做出决定。
3、送达(时限:1个工作日)
办理结果:根据申请人选择的送达方式发放行政许可决定书。
申请材料
1、1.监管信息;
2、1.1章节目录;
3、1.2备案表;>>备案表
4、1.3关联文件;
5、1.4符合性声明;>>承诺书
6、2.综述资料;
7、2.1章节目录;
8、2.2产品描述【2.2.1变更情况说明,2.2.2注册人名称变更(企业名称变更核准通知书和/或相应关联文件),2.2.3注册人住所变更(变更前后企业营业执照副本或事业单位法人证书复印件和/或相应关联文件),2.2.4境内体外诊断试剂生产地址变更(变更后的生产许可证及其附件,拟变更生产地址的现场检查报告)】;
9、3.需要说明的材料(委托生产适用);
10、3.1.1企业名称变更核准通知书(境内注册人或受托生产企业)和/或变更前后的营业执照,组织信用代码应前后一致。(委托生产适用)(注册人名称变更);
11、3.1.2委托生产合同(委托生产适用)(注册人名称变更);
12、3.1.3委托生产质量协议(委托生产适用)(注册人名称变更);
13、3.1.4知识产权保护协议(如适用)(委托生产适用)(注册人名称变更);
14、3.2.1受托人的生产许可证正、副本(委托生产适用)(医疗器械生产地址变更)(原受托企业生产地址变更情形);
15、3.2.2委托生产合同(委托生产适用)(医疗器械生产地址变更)(原受托企业生产地址变更情形);
16、3.3.1受托人的生产许可证正、副本(委托生产适用)(医疗器械生产地址变更)(新增受托企业情形);
17、3.3.2委托生产合同(委托生产适用)(医疗器械生产地址变更)(新增受托企业情形);
18、3.3.3注册产品的分类编码与受托企业生产范围不一致时还需提交医疗器械质量体系现场核查记录(委托生产适用)(医疗器械生产地址变更)(新增受托企业情形);
19、3.4.1拟更换受托人的生产许可证正、副本(委托生产适用)(医疗器械生产地址变更)(更换受托企业情形);
20、3.4.2委托生产合同(委托生产适用)(医疗器械生产地址变更)(更换受托企业情形);
21、3.4.3注册产品的分类编码与受托企业生产范围不一致时还需提交医疗器械质量体系现场核查记录(委托生产适用)(医疗器械生产地址变更)(更换受托企业情形);
22、3.4.4原委托终止合同(委托生产适用)(医疗器械生产地址变更)(更换受托企业情形)。
结果样本

常见问题
问题1:什么情况下需要申请体外诊断试剂注册证变更?
答:已注册的第二类、第三类医疗器械产品,其设计、原材料、生产工艺、使用范围、使用方法等发生实质性变化,有可能影响该医疗器械安全、有效的,注册人应向原注册部门申请办理变更注册手续。
本办事指南摘自药监局官网,如有变动,以官方发布为准。