年度质量回顾与 GMP 质量管理体系文件构建及组织要点解析
举办《年度质量回顾与GMP质量管理体系文件构建及组织要点解析》培训通知
2018 年 1 月 25 日-27 日(25 日报到) 成都市
1800 元/人(含教材费、证书费、会务费)。
![]()
一、举办背景
产品年度质量回顾分析是药品生产质量管理中的重要环节,是GMP认证关注的项目。对产品进行年度产品质量回顾分析,能够考察药品的生产工艺的状态,以确认工艺流程稳定可靠、质量标准的实用性,以及原辅料、中间产品、成品现行质量标准的适用性,能够及时发现不良趋势,从而确定出对产品及工艺控制过程进行改进的方向。
为帮助各药品生产企业,如何结合自身特点,深入细化地开展年度质量回顾和GMP质量管理体系文件管理工作,飞天教育将举办“年度质量回顾与GMP质量管理体系文件构建及组织要点解析”培训班,特邀各单位积极选派人员参加。现将有关事项通知如下:
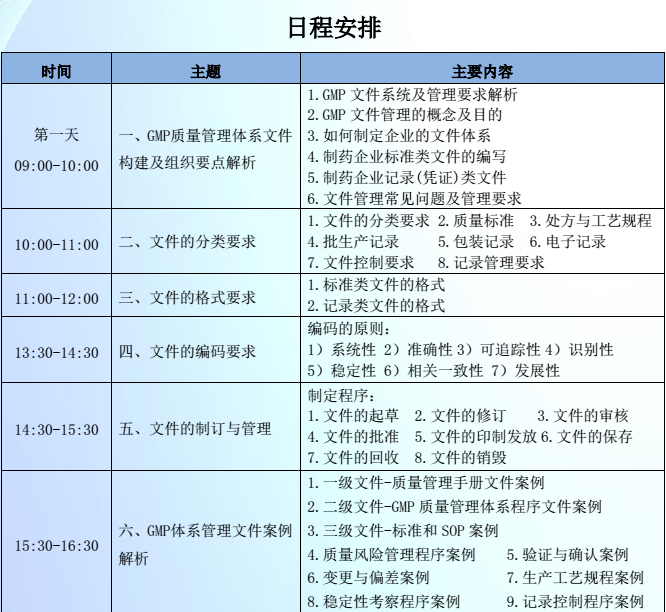
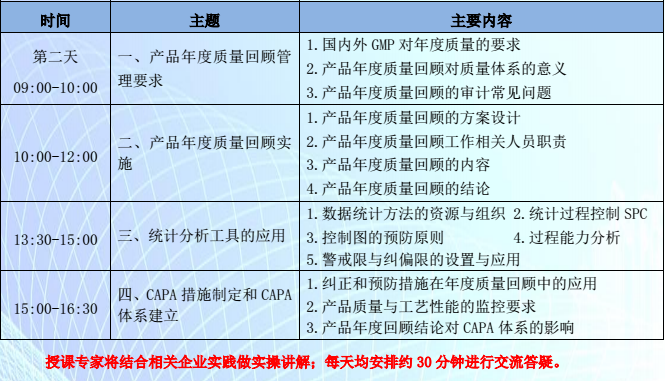
二、 会议内容(日程安排详见附件)
1.年度质量回顾常见问题与缺陷项目分析
2.年度质量回顾执行流程与CAPA的应用
3.统计分析工具与方法在年度质量回顾中的应用
4.GMP质量管理体系文件构建及组织要点解析
5.文件的分类要求
6.文件的格式要求
7.文件的编码要求
8.文件的制订与管理
9.GMP体系管理文件案例解析
主讲人:刘老师 国家食品药品监督管理局高级研修学院特聘讲师,飞天教育资深专家,曾任职国内知名药企及外资企业高管;具有近20年药物研发、GMP生产管理实践经验,亲自参加过多次FDA 、WHO、TGA和CEP认证及国内的检查。大量接触第一线的实际问题,具有丰富的分析问题和解决问题的能力和经验。
主讲人:张老师 飞天教育特聘专家,曾任职于国内知名药企质量总监,12年以上药品质量管理/国际注册经验。具有较全面的药品国际认证与质量管理经验。熟悉欧盟 GMP、FDA cGMP、ICH Q7,以及 ICH 、PIC/S 等指南。参与多家企业过无菌制剂厂房设计到GMP检查的全过程,具有验证及GMP审核方面的经验。
三、热门课题如下:
1、《生命周期方法的工艺验证和清洁验证实务》提高班
2、《药品生产全过程质量风险管理与统计分析》提高班
3、《药品共线生产风险控制与设施、设备要求及案例分析》专题培训班
4、《制药行业GMP质量管理与工艺验证数据统计分析应用与实践》提高班
5、《药品QC微生物实验室管理及技术应用》专题培训班
6、《飞行检查常态下的制药企业GMP维护与实践应用实务班》专题培训班
7、《符合新版GMP的设备预防性维护与计量管理》培训班
8、《制药企业飞行检查应用》实务班
9、《药品GMP计算机化系统验证》实操训练班
10、《实验室控制验证及GMP符合性》专题培训班
四、参会对象
制药企业、医药研发等相关专业人员;药品生产企业负责厂房、设施、设备的工程技术人员及质量管理人员、控制室人员、验证人员、法规事务部人员,生产部门负责人、车间主任及有关技术人员、生产副总;项目工程师,验证经理及QA人员。
咨询电话:17301029586 彭倩
报到通知(详细时间、地点、乘车路线等信息)将于开班前 5 天通知学员