PDF
¥ 39.00 ¥59.00
医疗器械注册人备案人开展
不良事件监测工作检查要点
相关推荐:

2021年4月9日,国家药监局发布了国家药监局综合司关于印发医疗器械注册人备案人开展不良事件监测工作检查要点的通知(药监综械管〔2021〕43号),明确了医疗器械注册人、备案人开展不良事件监测具体要求,强调落实医疗器械注册人备案人主体责任和加强医疗器械不良事件监测检查工作。
CIO在线帮您快速梳理检查要点,助力高效开展工作,科学规避风险,加深对质量管理体系的认识和理解。

本课件内含39页,主要从以下5个方面进行展开:
1、《医疗器械注册人备案人开展不良事件监测工作检查要点》实施背景
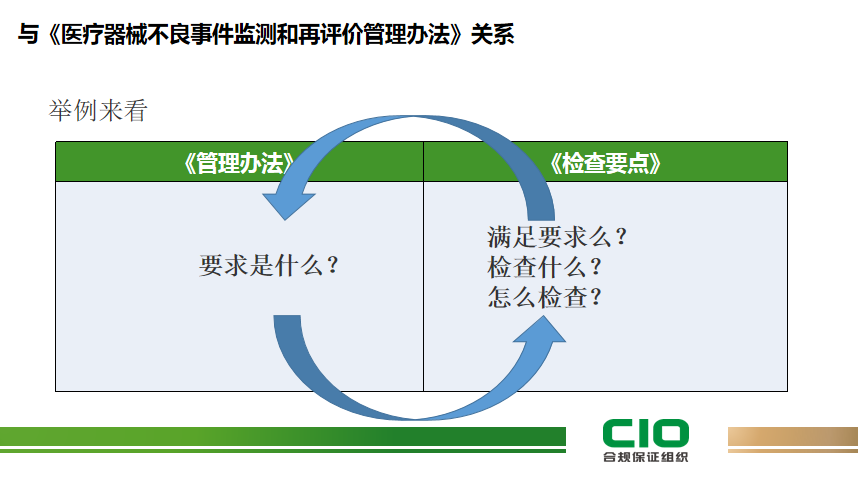
2、与《医疗器械不良事件监测和再评价管理办法》关系
3、分章讲解
•机构和人员
•文件管理
•设计开发
•不良事件监测分析和改进
4、医疗器械企业面临的挑战
5、医疗器械企业的先期准备
更多拓展内容可观看培训视频《百城行:医疗器械注册人备案人开展不良事件监测工作检查要点》。

1、高效及时
紧跟政策步伐,及时快速解读,助力企业高效开展工作。
2、视频教学
不受时空限制,随时随地听课,提升工作技能。
3、行业积淀
讲师多年行业经验,实时联系行业态势,深度精准指导。

1、可开发票
2、课件售出后,我们将安排专员进行实时跟踪回访,全程为您答疑!
3、若您在购买或使用课件过程中遇到任何问题,亦可点击“在线咨询”联系我们的客服。我们将竭诚为您解答,谢谢!
4、服务咨询热线:400-003-0818

本预览仅为部分内容,查看完整课件,请点击“立即下载”进行购买下载。